Как покрыть медью нержавейку. Гальваническое покрытие медью в домашних условиях
Процесс извлечения металла из раствора и нанесения его на поверхность металлическго изделия называется гальваностегией. Меднение — нанесение меди на поверхность металлического изделия.
Процесс меднения распространен в промышленности, и используется не только как самостоятельный процесс, но и как подготовительный процесс перед хромированием, никелированием и серебрением. Применение меднения, как подготовительной операции, связано с тем, что медь очень прочно держится на стали, выравнивает дефекты поверхности и другие металлы очень хорошо осаждаются на медь, а чистую сталь — плохо.
Меднение металлов в домашних условиях не такая сложная операция, есть два способа: с погружением в электролит и без.
Меднение металла с погружением в электролит.
Металлический предмет обработайте, как обычно,
наждачной бумагой, чтобы удалить оксидную пленку, протрите щеткой, как
следует промойте водой, обезжирьте в горячем содовом растворе и промойте
еще раз.
Раствор электролита для меднения: 20 г медного купороса и 2-3 мл серной кислоты на 100 мл воды — налейте в емкость, раствор должен полностью покрыть электроды. Пользуясь реостатом, установите ток от 10 до 15 мА на каждый квадратный сантиметр поверхности детали. Минут через двадцать выключите ток и выньте деталь — она покрыта тонким слоем меди. Чем дольше идет процесс, тем толще слой меди.
Меднение без погружения в электролит.
Этот процесс подходит не только для стали, но и для цинка и алюминия. С одного конца мягкого многожильного провода снимите изоляцию и растеребите тонкие медные проволочки, чтобы получилась медная кисть. Для удобства работы привяжите ее к деревянной палочке или карандашу, а другой конец провода подсоедините к положительному полюсу источника тока.
Для удобства работы привяжите ее к деревянной палочке или карандашу, а другой конец провода подсоедините к положительному полюсу источника тока.
Приготовьте электролит — концентрированный раствор медного купороса, желательно слегка подкисленный, — и налейте в широкую склянку, в которую удобно будет макать «кисть».
Подготовьте металлическию пластинку или другой небольшой предмет, желательно с плоской поверхностью. Протрите его мелкой наждачной шкуркой и обезжирьте, прокипятив в растворе стиральной соды. Положите пластинку в ванночку или кювету и подсоедините ее проводом к отрицательному полюсу источника тока. Схема собрана, осталось только ввести электролит.
Обмакните «кисть» в раствор медного купороса и проведите ею вдоль пластинки, стараясь не дотрагиваться до поверхности; работайте так, чтобы между пластинкой и кистью был всегда слой электролита. Проводки все время должны быть смочены раствором. На глазах пластинка будет покрываться красным слоем металлической меди.
Такой процесс, при котором деталь не опускают в электролитическую ванну, а обрабатывают снаружи небольшими участками, добавляя все время электролит, используют в тех случаях, когда деталь настолько велика, что для нее не подберешь подходящей ванны.
Мы переехали в новый офис — соседнее здание. Обращайте внимание на схему проезда в разделе контактов.
Вакуумные покрытия временно не наносим
В связи с модернизацией участка вакуумных покрытий, работы по вакуумным напылениям временно не выполняем.
Сертификат ISO 9000
Система менеджмента качества на нашем предприятии соответствует ISO 9000
Нанесение нитрида титана
Наносим вакуумным напылением нитрид титана (TiN) на изделия габаритами до 2500х2500х2500 мм.
Латунирование и бронзирование
Появилась возможность выполнения работ по декоративному нанесению латуни и бронзы
Хорошая новость! Мы переехали!
В связи с долгожданным расширением производства, мы переехали на новую площадку в г. Балашиха. Для вашего удобства — появилась возможность осуществлять забор/доставку деталей нашим автотранспортом!
Балашиха. Для вашего удобства — появилась возможность осуществлять забор/доставку деталей нашим автотранспортом!
Партнеры
- Шифры наносимых покрытий: М, М.б
- Обрабатываемые стали: любые, в том числе алюминиевые и титановые сплавы
- Габариты изделий: до 1000х1000х1000 мм. Масса до 1 т.
- Нанесение покрытий на изделия любой сложности
- ОТК, паспорт качества, работа в рамках ГОЗ
Общая информация
Меднение — это процесс гальванического нанесения слоя меди толщиной от 1 мкм до 300 мкм и более.
Медные покрытия обладают высоким сцеплением (адгезией) с различными металлами, высокой пластичностью и электропроводностью.
Области применения деталей с меднением зависят от того, используется ли медное покрытие как функциональное, или же медное покрытие выступает подслоем для нанесения других гальванических покрытий.
В атмосферных условиях медные покрытия легко окисляются и покрываются оксидой плёнкой, приобретая радужные разводы и пятна разных оттенков.
Основные области применения медных покрытий:
Использование меднения как самостоятельного покрытия
- В декоративных целях.
В настоящее время большой популярностью используются старинные медные изделия. Гальваническое меднение позволяет наносить медные покрытия, которые после специальной обработки «состариваются» и выглядят так, словно были изготовлены давно.
- В гальванопластике.
Гальваническое меднение применяется для изготовления металлических копий изделий различной формы и размеров. Создаётся восковая или пластиковая основа, которая покрывается электропроводящим лаком и, впоследствии, слоем меди.
Такая технология меднения часто используется при изготовлении сувениров, ювелирных изделий, барельефов, волноводов и матриц.
- В технических целях.
Большое значение меднение металла занимает в электротехнической области.
- При нанесении многослойных защитно-декоративных покрытий.
Как правило, в сочетании с никелем и хромом (трёхслойное защитно-декоративное покрытие) и другими металлами в качестве промежуточного слоя для повышения сцепления с металлом основы и получения более прочных и блестящих покрытий.
- Для предохранения участков при цементации.
Меднение часто используется для предохранения участков стальных деталей от цементации (науглероживания). Медью покрываются только те участки, которые в дальнейшем подлежат обработке резанием (твёрдые науглероженные поверхностные слои не поддаются такой обработке, а медь защищает покрытые участки от диффузии в них углерода).
- При ремонте и восстановлении изделий.
Меднение металла часто применяется в реставрационных работах при восстановлении хромированных частей автомобильной или мото-техники, при этом наносится большой слой меди 100-250 мкм и более, который закрывает поры и дефекты металла, шлифуется и выполняет роль новой основы для нанесения последующих покрытий.
Примеры деталей с гальваническим меднением
Технология меднения
Различают 2 типа медных электролитов: кислые и щелочные.
В кислых электролитах нельзя получить прочно сцепленные медные покрытия на стальных и цинковых изделиях, так как в этом случае железо и цинк в контакте с медью растворяются — нарушается сцепление с покрытием. Для устранения этой особенности — необходимо первый тонкий слой меди (2—3 мкм) нанести в щелочном электролите, а в дальнейшем наращивать покрытие в более экономичном кислом электролите до заданной толщины.
Цинковые изделия сложной формы меднить лучше всего в щелочных (цианистых) электролитах.
Кислые электролиты меднения
Наиболее распространены электролиты двух видов — сернокислые и борфтористоводородные .
Наибольшее применение нашли сернокислые электролиты, отличающиеся простотой состава, устойчивостью и высоким выходом по току (до 100%).
Перед меднением стальных деталей в кислых электролитах их предварительно меднят в цианистых электролитах или осаждают тонкий подслой никеля.
Недостатком этих электролитов является невозможность непосредственного покрытия стальных и цинковых деталей вследствие контактного выделения меди, имеющей плохое сцепление с основным металлом, а также их незначительная рассеивающая способность и более грубая структура осадков по сравнению с другими электролитами.
Щелочные электролиты меднения
К щелочным электролитам меднения относятся цианистые , пирофосфатные и другие электролиты.
Цианистые медные электролиты обладают высокой рассеивающей способностью, мелкокристаллической структурой осадков, возможностью непосредственного меднения стольных деталей.
К недостаткам относятся низкая плотность тока и неустойчивость состава вследствие карбонизации свободного цианида под действием двуокиси углерода воздуха. Кроме того, цианистые электролиты характеризуются пониженным выходом по току (не более 60-70%)
Стоимость меднения
Для оценки стоимости работ, просьба выслать запрос на электронную почту [email protected]
К запросу желательно приложить чертёж или эскиз изделий, а также указать количество деталей.
Меднение – это процесс нанесения на поверхность медного слоя гальваническим способом.
Медный слой придает изделию внешнюю привлекательность, что позволяет использовать прием гальванического покрытия медью в дизайнерских проектах. Также он придает металлу высокую электропроводность, что позволяет подвергать изделие дальнейшей поверхностной обработке.
Меднение можно использовать в качестве основного процесса для создания поверхностного слоя, а также как промежуточную операцию для дальнейшего нанесения другого металлического слоя. К такому способу можно отнести, например, процесс серебрения, хромирования или никелирования.
К такому способу можно отнести, например, процесс серебрения, хромирования или никелирования.
Меднение можно проводить в домашних условиях. Это дает возможность решить много бытовых проблем.
Гальваника в домашних условиях: оборудование и материалы
Чтобы выполнить покрытие медным слоем самостоятельно, нужно приобрести необходимое для процесса оборудование и материалы.
Прежде всего, нужно подготовить источник электрического тока. Разные домашние мастера советуют использовать силу тока, разброс которой в большом диапазоне. Работа должна проводиться на постоянном токе.
В качестве источника тока можно взять батарейку КБС-Л напряжением 4,5 вольт или новую батарейку марки «Крона» с рабочим напряжением 9 вольт. Можно также вместо нее использовать выпрямитель малой мощности, дающий напряжение не более 12 вольт, или автомобильный аккумулятор.
Обязательным является использование реостата для регулировки напряжения и плавного выхода из процесса.
Для раствора электролита должна быть заготовлена нейтральная емкость, например из стекла, а также пластиковая широкая посуда, имеющая достаточные размеры для размещения в ней детали. Емкости должны выдерживать температуру не менее 80оС.
Емкости должны выдерживать температуру не менее 80оС.
Также понадобятся аноды, обеспечивающие покрытие всей поверхности детали. Они предназначены для подведения тока в электролитный раствор и его распределение по всей площади детали.
Для проведения гальваники в домашних условиях понадобятся также химреактивы для приготовления раствора:
- медный купорос,
- соляная или другая кислота,
- дистиллированная вода.
Заготовив все необходимое, можно приступать к работе.
Меднение стальных изделий
Меднение стали медным купоросом является одним из основных процессов в области гальваники потому, что оно используется для предварительного покрытия медью. Она отличается высокой адгезией к стальной поверхности, в отличие от других металлов, которые не обладают хорошим сцеплением со сталью. Медный слой при соблюдении технологии держится на стальных изделиях прекрасно.
Есть две технологии нанесения покрытия: с погружением изделия в электролитный раствор и способ неконтактного покрытия поверхности медью без помещения в жидкий электролитный раствор.
Меднение путем погружения в раствор
Процесс выполняется с соблюдением следующих этапов:

Покрытие медью без помещения в электролитный раствор
Такой способ используется не только для стальных изделий, но и алюминиевых предметов и изделий из цинка. Процесс осуществляется так:

Между поверхностью детали и импровизированной медной кистью всегда должен быть слой из раствора электролита, поэтому кисть необходимо обмакивать в электролит постоянно.
Меднение алюминия медным купоросом
Нанесение на поверхность меди – отличный способ обновления алюминиевых столовых приборов и других изделий из алюминия, используемых дома.
Меднение алюминия медным купоросом можно провести самостоятельно. Упрощенный вариант для демонстрации процесса – это покрытие медью алюминиевой пластинки простой формы.
На этом примере можно потренироваться. Выполнение процесса происходит так:
Выполнение процесса происходит так:
1. Поверхность пластинки необходимо сначала зачистить, а затем обезжирить.
2. Затем нужно нанести на нее немного концентрированного раствора сернокислой меди (медного купороса).
3. Следующим действием является подсоединение к алюминиевой пластинке провода, подсоединенного к отрицательному полюсу. Подсоединять провод к пластинке можно с помощью обычного зажима.
4. Положительный заряд подается на устройство, состоящее из оголенного медного провода с диаметром от 1 до 1,5 мм, конец которого распределяется между щетинами зубной щетки.
Во время работы этот конец провода не должен касаться поверхности алюминиевой пластины.
5. Обмакнув щетину в раствор медного купороса, начинают водить щеткой в подготовленном для покрытия медью месте. При этом не нужно допускать замыкания цепи, прикасаясь к поверхности алюминиевой пластины концом медного провода.
6. Омеднение поверхности сразу становится визуально заметно. Чтобы слой был качественным, с окончанием процесса не нужно торопиться.
Чтобы слой был качественным, с окончанием процесса не нужно торопиться.
7. После завершения работы слой меди нужно выровнять дополнительной очисткой, удалив остатки медного купороса и протерев поверхность спиртом.
Гальванопластика в домашних условиях
Гальванопластикой называют процесс электрохимического воздействия на изделие с целью придания ему необходимой формы осаждаемым на поверхности металлом.
Обычно эту технологию используют для покрытия металлом неметаллических изделий. Широко применяют ее в ювелирной области и дизайне бытовых предметов.
Покрытие рабочего изделия должно обладать электропроводящими свойствами. При отсутствии такого слоя сначала предмет покрывают графитом или бронзой.
Основными металлами, используемыми для гальванопластики, являются медь, никель, серебро и хром. Также используют металлизацию поверхностей сплавами из стали.
Гальванопластика в домашних условиях особенно популярна среди мастеров. Чтобы создать нужную форму, с копии делается ее слепок. Для этого используют легко плавящийся металл, графит и гипс.
Чтобы создать нужную форму, с копии делается ее слепок. Для этого используют легко плавящийся металл, графит и гипс.
После изготовления формы предмет подвергают покрытию металлом с использованием электролита.
Для того чтобы подготовить металлический предмет к дальнейшей обработке, его нужно покрыть медью — такой процесс называют гальваностегией. Принцип его действия заключается в осаждении на поверхность обрабатываемой детали из другого металла, который растворен подходящим средством. Из данной статьи вы узнаете, как покрыть медью металл в домашних условиях, чтобы реализовать все последующие свои задумки с заготовкой.
Для чего это нужно?
Технология гальваностегии включает в себя создание раствора и образование различных электродов. Во время этого процесса медные ионы, которые растворены в электролите, притягиваются минусовым полюсом обрабатываемой детали на свою поверхностную точку.
Гальваностегия металлических деталей в промышленности применяется не только как завершающий обрабатывающий процесс. Она может применяться для того, чтобы подготовить детали к последующей операции (к примеру, хромированию, никелированию, серебрению каких-либо предметов).
Она может применяться для того, чтобы подготовить детали к последующей операции (к примеру, хромированию, никелированию, серебрению каких-либо предметов).
В домашних условиях чаще всего проводится химическое меднение деталей. Также стоит заметить, что есть множество способов проведения такой процедуры, каждый из которых имеет свои преимущества и недостатки.
Сферы использования гальваностегии
Покрывать медью металл в домашних условиях в последнее время стало очень полезно. Чаще всего к такой процедуре подходят в следующих целях:
- В декоративных. Например, таким способом состаривают различные детали для того, чтобы придать винтажный вид.
- В гальванопластике. Очень часто наносят медный слой на сувениры, ювелирные украшения.
- В отрасли техники. Это связано с низкой стоимостью омеднения.
- Для нанесения защитно-декоративной прослойки того или иного изделия.
- Для того чтобы реставрировать или восстанавливать какие-либо детали.
Гальваностегия электролитным раствором
Таким способом можно покрыть медью сталь в домашних условиях, а также другие детали за исключением алюминия и цинка.
Для дальнейшей процедуры необходимо подготовить следующие материалы:
- Небольшие пластины из меди.
- Токопроводящая проволока (лучше запастись несколькими метрами).
- Источник тока, напряжение которого не должно быть более, чем 6 В.
- Реостат, чтобы регулировать ток.
- Амперметр.
- Электролит.
Важно! Последний компонент можно приобрести в специальном магазине, а можно и изготовить самостоятельно. Для этого нужно сделать раствор серной кислоты и дистиллированной воды при соотношении 2/100 мл. Нужный раствор получится, когда вы добавите к составу не больше 20 г медного купороса.
Суть работы заключается в следующем:
- Очистить обрабатываемую деталь наждачной бумагой — это нужно для того, чтобы снять оксидную пленку. Далее покрыть медью металл в домашних условиях будет не так трудно.
- Обезжирить металлическим предмет горячим раствором соды, промыть его чистой водой.
- В подходящую по объему емкость из стекла налить приготовленный электролит.

- Опустить в жидкость две пластины из меди на подготовленных токопроводящих проводках. Между двумя пластинками из меди подвешивается уже обезжиренная деталь на таком же проводке.
Важно! Проследите за тем, чтобы пластины из меди были полность погружены в электролит.
- Далее концы проводов от пластин из меди присоединяются к положительной клемме источника тока, а деталь — к отрицательной. Далее в созданную электросеть нужно подключить амперметр с реостатом. После того, как ток подключится к цепи, реостатом нужно установить его примерно 15 мА на 1 см площади детальной поверхности.
- Далее деталь выдерживается примерно 15-20 минут.
- По истечении времени нужно отключить электропитание и вытащить обрабатываемый металл из раствора.
В конечном итоге вы заметите, что смогли покрыть медью металл в домашних условиях, ведь он полностью покроется тонкой блестящей пленкой.
Важно! Толщина медного слоя будет зависеть от того, как долго была выдержана деталь в электролите.

Гальваностегия другим способом
Данный способ отлично подойдет для металлов-исключений, что были названы ранее — цинка и алюминия.
Алгоритм работы:
- Вооружиться многожильным проводом из меди, снять изоляцию с обоих его концов.
- Растеребить мягкий провод с одной стороны, получив имитированную кисточку. Привязать к этому концу предмет, похожий на рукоятку.
- Противоположную сторону провода необходимо соединить к плюсовой клемме источника электротока.
Важно! Напряжение должно быть не более, чем 6 В.
- Подготовить электролит описанным выше способом, вылить его в широкую тару — это нужно для удобства макания туда “кисточки”.
- Положить внутрь подготовленной емкости небольшую деталь из металла. Соединить ее, используя при этом провод, к отрицательной клемме токового источника также с напряжением 6 В.
Важно! Деталь должна быть предварительно очищена и обезжирена.

- Процесс покрытия алюминия медью в домашних условиях заключается в следующем: кистообразный конец провода нужно промакивать электролитным раствором и проводить им по поверхности обрабатываемого металлического предмета, не касаясь его. Дальше — отрицательно заряженный металл притянет к себе медные ионы и ее поверхность приобретет медную пленку.
Важно! Следите за тем, чтобы между концом растеребленной проволоки и металла был маленький слой электролитного раствора (и катод, и анод обязательно должны быть смочены этим раствором).
Меднение – это технологический процесс, позволяющий наносить на металл, а также другие материалы слой меди толщиной от 1 до 300 мкм. Покрытие медным слоем обеспечивает хорошую адгезию покрытий и при увеличении толщины покрытий придает блеск изделиям, устраняет небольшие дефекты, позволяет создавать копии вещи. Удивительно, но все это можно делать и самим. Сегодня мы расскажем, как осуществить меднение в домашних условиях.
Гальваника медью в домашних условиях: общие сведения
С технической точки зрения обработка – это электрохимический процесс. В процессе всегда есть два «участника» анод+электролит (источник металла) и деталь.
Технология процесса достаточно проста. Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Среди основных этапов:
- Подготовка поверхности (механическая и химическая).
- Нанесение подслойного покрытия (если необходимо)
- Меднение в соответствующем исходному металлу электролите.
Для декоративного гальванического меднения подойдут электролиты матового и блестящего меднения. После нанесения слоя, можно обработать поверхность в электролитах серебра, золота никеля и т.д.
Необходимые инструменты
«Ингредиенты», без которых процесс не состоится, реально подготовить самим. Наши специалисты
утверждают, что прежде всего, нужны:
- Источник постоянного тока.
 Выбирается в зависимости от размера изделия.
Выбирается в зависимости от размера изделия. - Аноды. Анодные пластины выполняют несколько функций. В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
- Рабочий электролит. Кислотный, щелочной или пирофосфорный раствор. Состав электролита выбирается в зависимости от исходного металла. Необходимо помнить, что любой электролит не универсален и подойдет не для всех работ.
Подготовка материала
Как правильно подготовить простой электролит меднения.
Стоит отметить, что химические реактивы для меднения найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
- Дистиллированная вода (или бидистиллят).
- Медный купорос.
- Соляная или другая кислота.

Готовый раствор имеет яркий синий цвет, запаха нет. Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах. Обязательно следует указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.
Подготовка материала
Химическое меднение является альтернативой электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды материалов подвергаются очистке по-разному:
- Сталь .
 Обезжиривать сталь можно раствором из едкого натрия и едкого калия при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
Обезжиривать сталь можно раствором из едкого натрия и едкого калия при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
- Медь и сплавы. Обезжиривание осуществляется едким натрием, нагретым предварительно до 40°, около 10 минут.
- Чугун. Для процесса обезжиривания нужен раствор из едкого натра, жидкого стекла, карбоната натрия и фосфата натрия при нагревании до 90°.
- Вольфрам. Меднение вольфрама в домашних условиях начинается с чистки предмета от грязи и прочих дефектов наждачной бумагой.
Техника безопасности
Несмотря на возможность гальваники в домашних условиях, процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому следует неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью дома – работайте только в нежилом, хорошо проветриваемом помещении. Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты нужно:
- Постоянно быть в респираторе, чтобы обезопасить дыхательные пути. лучше всего использовать вытяжку.
- Защитить руки прочными прорезиненными перчатками.
- Надеть специальную форму или клеенчатый фартук, противоожоговую обувь.
- Не забыть очки для безопасности зрительных органов.
- Не приносить в помещение еду и питье.
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Гальваника в домашних условиях: меднение
Почему в гальванике столь востребована именно медь? Она имеет высокую адгезию (иными словами – сцепление) к самым разным материалам. Это значит, что она превосходно держится на стальных и прочих изделиях, не отлетая и не скалываясь.
Медь – красивый яркий металл, внешне напоминает самородки розово-красного оттенка. Материал проводит не только тепло, но и электрический ток – отсюда и высокий спрос в сфере электротехники и приборостроении. Однако чистую медь найти сложно. Чаще она поставляется с различными примесями.
Медные покрытия:
- Отличаются малым сопротивлением, что используется в электротехнике
- Скрывает мелкие недочеты поверхности.
- Быстро окисляется, что используют для получения эффекта «антик».
Технологий нанесения покрытия существует две. Одна происходит путем погружения изделия в раствор электролиты (с подачей тока или без). Второй же способ – это метод селективного нанесения покрытия без погружения в раствор. Рассмотрим оба.
Метод погружения
Поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
- Анодную пластину (можно две) помещают в емкость, которую будем называть ванной.
 На аноды замыкают положительную клемму.
На аноды замыкают положительную клемму. - Между анодами на любом удобном проводнике подвешивается деталь, к ней подводят отрицательный полюс от блока питания.
- Готовый раствор вливается в ванночку – при этом уровень покрытия должен быть выше, чем расположена деталь.
- После подключения электродов к источнику тока выставляют рабочий ток. Это примерно 1 А/кв.дм. покрытия.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Покрытие без погружения
Данный способ имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшие толщины покрытий. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Порядок действий:
- Готовят «тампон» для нанесения покрытия. Берут медный проводник и наматывают кусок искусственной ткани (полиэстер подойдет).
- Противоположный конец проводника подсоединяют к положительной клемме источника напряжения.

- Электролитным раствором наполняют емкость – так удобнее окунать карандаш.
- Деталь аккуратно очищают и обезжиривают, а потом помещают в пустую ванночку. Там изделие подсоединяется к отрицательной клемме.
- Тампон смачивают в растворе. Затем им проводят по поверхности изделия, закрашивая ее постепенно.
Процесс длится до момента покрытия медным слоем изделия.
Особенности гальванопластики
Гальванопластика — это процесс нанесения меди на проводящую или непроводящую поверхность изделия с последующим снятием покрытия с негативной матрицы. Таким образом можно получить множество очень точных копий с одного изделия. При этом требуется наращивание меди толщиной не менее 200 мкм, чтобы изделие получилось прочным.
Важно учесть, что, если поверхность изделия не имеет свойств проводника, то потребуется больше усилий – а именно, особое предварительное покрытие графитом, серебром или медью. Основным материалом для осуществления гальванопластики традиционно считается медь, но можно выращивать матрицы из серебра чистотой 9999.
Обучение гальванике
Можно сделать вывод, что меднение сегодня — это один из наиболее актуальных гальванотехнических процессов, обучиться которому может каждый. Компания «6 микрон» проводит обучение по направлению «Гальваника» для всех желающих! Вы сможете выбрать удобную для Вас программу обучения, которая лучше всего подойдет под Вашу техническую задачу. Все интересующие вопросы можно задать по телефону или по электронной почте, наши технологи помогут Вам определиться с подходящим курсом для обучения.
Видео руководство по меднению деталей в домашних условиях:Меднение в домашних условиях: гальваника своими руками
Медный купорос нашел широкое применение, не только доя обработки плодовых деревьев и кустарников. Гальванопластика дома используется для защитного и декоративного покрытия металлов медью.
Меднение в домашних условиях не требует сложного
оборудования. Наряду с покрытием, гальванопластика позволяет получать
уникальные украшения из неметаллических форм.
Гальваника своими руками отличается доступностью в любом возрасте. Она ориентирована на недорогие простые компоненты, которые без труда всегда можно приобрести.
Гальванопластика дома
Гальваника относится к одному из разделов электрохимической науки. В ее ведении находится изучение и практическое применение осаждения ряда веществ на любую поверхность. Она имеет два родственных направления: гальваностегию и гальванопластику, которые имеют незначительное отличие.
В том и другом случае применяется осаждение металлов на какую-либо поверхность. Под гальванопластикой понимается процесс создания точной копии той или иной детали, когда для покрытия используется медь.
Нередко меднение осуществляется перед серебрением, никелированием или хромированием изделий. Причина в том, что без предварительной подготовки некоторые металлы плохо удерживаются, например, на стальной поверхности.
Различают
технологические или декоративно-защитные покрытия гальваники, которые
представляют тонкий слой металла, служащий эстетическим целям. Гальванопластика
дома не повышает прочность изделия, но для изящности и придания «свежего вида» вполне
соответствует.
Гальванопластика
дома не повышает прочность изделия, но для изящности и придания «свежего вида» вполне
соответствует.
Почему медь как металл для покрытия наиболее востребован? В первую очередь этот металл имеет высокое сцепление, то есть адгезию с различными материалами. Медное покрытие прекрасно держится на деталях из стали, вольфрама, не отлетает и не скалывается.
К тому же, медь яркий и превосходного вида материал. Она внешне похожа на самородки розовато-красного цвета. Металл отличается высокой теплопроводностью и оказывает малое препятствие прохождению электротоку, на основании чего востребован в приборостроении и электро- и радиотехнике.
Медные покрытия неплохо скрывают неровности
поверхностей, но быстро окисляются, что нашло применение в эффекте
«антик». В то же время, образование
патины, например, на декоративной кованой ограде, придает ей особенный вид.
Однако в первозданном виде медь практически отсутствует. По большей части в ней
присутствуют разные примеси.
В то же время, образование
патины, например, на декоративной кованой ограде, придает ей особенный вид.
Однако в первозданном виде медь практически отсутствует. По большей части в ней
присутствуют разные примеси.
Гальванопластика дома опирается на слой меди, образованный на разных предметах, посредством электролита с медным купоросом. Технология гальванопластики в домашних условиях осуществляется как с пропусканием через электролит постоянного электротока, так и без его наличия. Поэтому гальваника своими руками химическим методом интересна тем, что какие-либо навыки не потребуются.
Химическое покрытие без электролиза
Способ меднения стальных деталей без электрического тока является наиболее простым, недорогим и доступным. Химическое покрытие без электролиза проводится с использованием следующих материалов:
сернокислая медь;
электролит для аккумуляторов или серная кислота;
дистиллированная вода;
пищевая сода;
щелочное средство для мытья посуды;
спирт и
растворитель.
Из инструментов и оборудования понадобятся:
угловая шлифовальная машина («болгарка») и шуруповерт;
очки для защиты глаз и перчатки из резины;
металлическая губка для мытья кухонной утвари;
стеклянная или пластиковая тара;
проволока, наждачка, ветошь.
Химический способ не позволяет создавать покрытия предметов толстым слоем меди. Однако благодаря ему, кроме металлов, легко получаются декоративные пленки на керамике, стекле, пластике и других материалах самостоятельно в неподготовленной обстановке.
Приготовление рабочего раствора
Во главе угла процесса участвует медный купорос, который всегда доступен в отделах для садоводов и огородников торговых точек. Электролит и дистиллированная вода являются не отменными атрибутами магазинов запчастей для автомобилей. Остальные компоненты также не относятся к дефицитным.
Особое внимание
следует уделить качеству медного купороса. Когда на его упаковке не указывается
состав, то приготовление рабочего раствора электролита из такого продукта
вызывает сомнение. Не исключено, что он может содержать разные добавки,
несовместимые с процедурой меднения.
Когда на его упаковке не указывается
состав, то приготовление рабочего раствора электролита из такого продукта
вызывает сомнение. Не исключено, что он может содержать разные добавки,
несовместимые с процедурой меднения.
Вначале в стеклянной емкости, например, объемом 0,5 л растворяется 100 г медного купороса в 150 мл теплой (40 градусов) дистиллированной воды. Сырая водопроводная вода, используемая для бытовых нужд в домашних условиях, включает дозы хлорных соединений, влияющие на качество рабочего раствора. Для ускорения и тщательного перемешивания до окончательного растворения порошка используется шуруповерт с самодельной насадкой.
В приготовленную жидкость доливается 50 мл спирта и после перемешивания добавляется 250 мл электролита, представляющего 40-60 % раствор серной кислоты. Состав еще раз тщательно перемешивается и на этом приготовление рабочего раствора заканчивается.
Дополнительно
подготавливается две промывочных жидкости. В одной такой таре в 1 л чистой воды растворяется 2
столовых ложки пищевой соды для нейтрализации кислоты.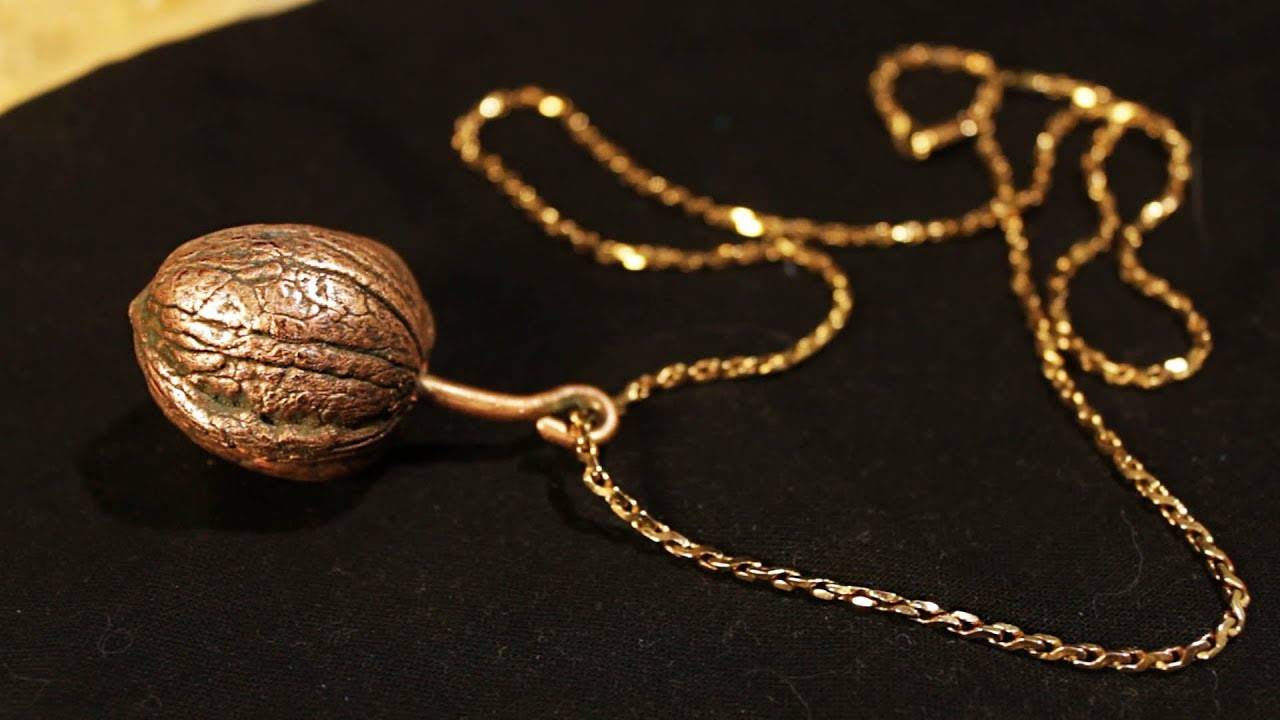 В другой емкости также в
1 л воды растворяется 2-3 столовых ложки порошка чистящего средства на щелочной
основе.
В другой емкости также в
1 л воды растворяется 2-3 столовых ложки порошка чистящего средства на щелочной
основе.
Меднение деталей
Прочное сцепление меди с другими металлами достигается, когда поверхность хорошо отшлифована и обезжирена. Для этой цели используется «болгарка», мелкая наждачная бумага и растворитель.
Кроме того, следует принять во внимание, что меднение деталей из стали усложняется, если они имеют защитное напыление, например, из цинка, к которому плохо пристает медь. К таким изделиям относятся болты, шайбы, гайки и другие, с которых предварительно нужно удалить покрытие.
Его удаление осуществляется многими способами, как например, с помощью того же электролита для кислотных аккумуляторов. Достаточно деталь поместить в него на несколько минут, а затем протереть ветошью, смоченной в растворителе.
Затем изделие
обезжиривается в щелочном растворе моющего средства с помощью металлической
губкой для мытья посуды и вытирается насухо. Непосредственно меднение деталей
осуществляется при помещении их на несколько секунд в рабочий раствор.
Непосредственно меднение деталей
осуществляется при помещении их на несколько секунд в рабочий раствор.
Тонкий слой меди на поверхности образуется практически в одно мгновение, и процедура повторяется несколько раз. Всякий раз изъятие детали из рабочего раствора заканчивается промывкой ее в содовом растворе, нейтрализующем кислоту.
Очередное окунание изделия в рабочий раствор желательно начинать со щелочного раствора и протиркой его насухо. Отсюда очевидно, что чем дольше деталь покрыта рабочим раствором, тем плотнее образуется медное покрытие.
После меднения деталей наступает момент полировки их поверхности. Однако слой меди быстро окисляется на воздухе, и изделие защищается путем покрытия его, например, хромом или серебром, в крайнем случае, лаком.
Меры предосторожности
Нередко при
различных работах, проводимых в домашних условиях, о технике безопасности
упоминается мимоходом. Однако в гальванике своими руками требуется обращать
пристальное внимание на меры предосторожности.
В технологии гальваники металлов опасность обусловлена применением токсичных химических препаратов, повышенной температуре растворов и последствиями электрохимических реакций. В первую очередь, когда используется концентрированная кислота, всегда следует добавлять ее небольшими порциями в воду, но не наоборот.
При покрытии деталей медью выделяется в небольшом объеме водород и другие газы. Поэтому наиболее пригодным местом проведения работ является гараж, мастерская или другие помещения, которые обязательно проветриваются или оборудованные системой вентиляции.
В технологии с подачей электрического тока, когда используется напряжение электросети, то обязательно соблюдать правила электробезопасности. В любом случае пристальное внимание следует уделить надежному заземлению оборудования и, в частности, гальванике в домашних условия, которая осуществляется в среде с повышенной влажностью.
Меры
предосторожности при использовании агрессивных химических средств ограждают от
непредсказуемых последствий. Так, например, при не осторожном обращении с
электролитом можно получить серьезные химические ожоги. Поэтому при
соприкосновении его с кожей необходимо тут же обработать пораженный участок
раствором соды.
Так, например, при не осторожном обращении с
электролитом можно получить серьезные химические ожоги. Поэтому при
соприкосновении его с кожей необходимо тут же обработать пораженный участок
раствором соды.
К общим мерам личной безопасности относятся следующие мероприятия:
наличие респиратора для ограждения дыхательных путей от выделяемых летучих веществ и газов;
для защиты зрения работы проводить в специальных защитных очках;
следует прикрывать руки и запястья прочными и надежными перчатками из резины с длинными раструбами;
ответственно относиться к выбору обуви, ограждающей от ожогов;
одежда должна быть прикрыта клеенчатым фартуком;
в процессе мероприятий воздержаться от употребления напитков и пищи, чтобы опасные вещества не проникли в тракт пищеварения.
Несмотря на то, что по токсичности медный купорос относится к 3 классу, обращение с ним также предусматривает определенных мер личной безопасности.
Таким образом,
меднение в домашних условиях без электролиза экономически выгодный способ,
отличается простотой и доступен при отсутствии соответствующих навыков. Гальваника своими руками в домашних условиях позволяет осуществлять защитное
покрытие металлов и в состоянии стать первичным толчком в увлекательный мир
гальванопластики для более серьезных изысканий.
Гальваника своими руками в домашних условиях позволяет осуществлять защитное
покрытие металлов и в состоянии стать первичным толчком в увлекательный мир
гальванопластики для более серьезных изысканий.
Как покрыть слоем меди металлические изделия: tvin270584 — LiveJournal
Многие хозяева заинтересованы в том, чтобы покрыть инструменты или какие-то отдельные метизы слоем меди. Покрытие медным слоем обеспечивает хорошую защиту металла, устраняет небольшие дефекты, придает блеск изделиям. Удивительно, но все это можно делать и самим. Сегодня мастер сантехник расскажет, как осуществить меднение металла в домашних условиях.
Состав меди
Металлическая медь представляет собой тяжелый металл розово-красного цвета, ковкий и мягкий, который плавится при температуре больше 1080°C, очень хорошо проводит теплоту и электрический ток: электропроводимость меди выше в 1,7 раза, чем алюминия и больше в 6 раз выше, чем железа, и только немного уступает электропроводимости серебра.
Специфические особенности меди определяются содержанием в металле конкретных примесей, количество которых может различаться приблизительно в 10 – 50 раз. По содержанию кислорода принято использовать следующую классификацию меди:
- Бескислородная медь с содержанием кислорода меньше 0,001%;
- Медь рафинированная с содержанием кислорода от 0,001до 0,01%, но с увеличенным присутствием фосфора;
- Медь большой чистоты с содержанием кислорода примерно 0,03-0,05%;
- Металл общего назначения с содержанием кислорода 0,05 – 0,08%.
В меди кроме кислорода может присутствовать водород, который в металл попадает в процессе электролиза или при совершении отжига в атмосфере, которая содержит водяной пар. При высокой температуре водяной пар разлагается с формированием водорода, который в медь легко диффундирует.
Атомы водорода в бескислородной меди размещаются в междоузлиях кристаллической решетки и на свойствах металла особо не сказываются. В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с закисью меди, при этом образуется в толще меди водяной пар, которому присуще высокое давление, что приводит к вздутиям, трещинам и разрывам. Это явление носит название «водородная болезнь».
В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с закисью меди, при этом образуется в толще меди водяной пар, которому присуще высокое давление, что приводит к вздутиям, трещинам и разрывам. Это явление носит название «водородная болезнь».
Железо, висмут, сурьма и свинец ухудшают пластичность меди. Примеси, что являются малорастворимыми в меди (свинец, кислород, сера, висмут), провоцируют хрупкость при высокой температуре, что затрудняет процесс горячей обработки давлением.
Физические свойства меди
Основное свойство меди, определяемое её использование, — высокая электропроводность или малое удельное электрическое сопротивление. Подобные примеси как железо, фосфор, мышьяк, олово и сурьма, значительно ухудшают её электрическую проводность. На величину электропроводности оказывает большое влияние механическое состояние меди.
Второе важное свойство меди – значительная теплопроводность. Легирующие добавки и свойства уменьшают теплопроводность меди, поэтому созданные на медной основе сплавы самой меди значительно уступают по этому показателю.
Легирующие добавки и свойства уменьшают теплопроводность меди, поэтому созданные на медной основе сплавы самой меди значительно уступают по этому показателю.
Медь при нормальных температурах является коррозиционно устойчивой в таких средах, как пресная вода, сухой воздух, морская вода при небольшой скорости движения воды, неокислительные кислоты и растворы соли при отсутствии кислорода, сухие галогенные газы, щелочные растворы за исключением солей аммония и аммиака, органические кислоты, фенольные смолы и спирты.
В аммиаке, хлористом аммонию, окислительных минеральных кислотах и растворах кислых солей медь не устойчива. Её коррозионные свойства также заметно ухудшаются в некоторых средах с возрастанием количества примесей. Допускается контакт меди с её сплавами, с оловом, свинцом во влажной атмосфере, морской и пресной воде. В то же время контакт меди с цинком и алюминием не допускается вследствие их быстрого разрушения.
Медь, ее сплавы и соединения нашли широкое применение в разных отраслях промышленности. Медь в электротехнике используют в чистом виде в производстве шин контактного и голого проводов, кабельных изделий, электрогенераторов, телефонного оборудования и радиоаппаратуры. Из меди изготавливают вакуум-аппараты, теплообменники и трубопроводы.
Сплавы меди с различными металлами используют в автомобильной промышленности и для изготовления химических аппаратов. Проволока из красной меди изготовления всевозможных шнуров и выгибания самых сложных элементов. Высокие свойства меди делают ее незаменимой при производстве филигранных деталей.
Использование меднения
В большинстве своем гальваническое меднение металлов используют в таких случаях:
- В декоративных целях. Огромной популярностью в настоящее время пользуются старинные изделия из меди. Процедура меднения позволяет наносить на металл медные покрытия, которые как бы «состариваются» после специальной обработки и выглядят так, будто изготовлены давным-давно.

- В гальванопластике. Используется гальваническое меднение железа для создания металлических копий изделий разной формы и различных размеров. Создаётся пластиковая или восковая основа, которую покрывают электропроводящим лаком и слоем меди. Подобную технологию меднения часто используют при изготовлении ювелирных изделий, сувениров, барельефов, матриц и волноводов.
- В технических целях. Меднение металла большое значение имеет в электротехнической области. Благодаря низкой стоимости меднения по сравнению с покрытиями золотом или серебром, медные покрытия нашли применение при изготовлении электротехнических шин, электродов, контактов и прочих элементов, которые работают под напряжением. Меднение зачастую используется как покрытие под пайку.
Меднение применяется в сочетании с прочими гальваническими покрытиями:
- При нанесении многослойного защитно-декоративного покрытия. Как правило, медь используется в сочетании с хромом и никелем (3-слойное защитно-декоративное покрытие) и прочими металлами как промежуточный слой для увеличения сцепления с основным металлом и получения более прочного и блестящего покрытия.

- Для предохранения участка при цементации. Меднение свинца способно предохранять участки стальных изделий от цементации — науглероживания. Покрывают медью исключительно те участки, которые подлежат в будущем обработке резанием. Твёрдый науглероженный поверхностный слой не поддается подобным обработкам, а медь может защитить покрытые участки от процесса диффузии углерода в них.
- При восстановлении и ремонте деталей. Меднение металла является важной процедурой при работах реставрационного характера и восстановлении хромированных частей мотто- и автомобильной техники. Наносить принято значительный слой меди – порядка 100-250 мкм и больше, который закрывает дефекты металла и поры и выполняет функции новой основы для последующих покрытий.
Процедура меднения
Меднением называют процедуру гальванического нанесения меди, толщина слоя которой составляет 1 — 300 мкм и больше. Меднение стали является одним из важнейших процессов в гальванике, что применяется в качестве предварительного процесса при подготовке металлической поверхности для покрытия другими металлами – при хромировании, никелировании и покрытии серебром, а также как законченный самостоятельный процесс.
Использование меднения как подготовительной манипуляции связано с тем, что этот металл способен очень прочно держатся на стали, выравнивать дефекты поверхности. Другие материалы на медь хорошо осаждаются, а вот на чистую сталь – не очень.
Медные покрытия характеризуются высоким сцеплением с разными металлами, высокой электропроводностью и пластичностью. Их принято наносить на стальные, цинковые и алюминиевые детали.
Только что нанесённое покрытие меди имеет ярко-розовый матовый или блестящий цвет, зависимо от технологии нанесения. Медные покрытия в атмосферных условиях способны легко окисляться и покрываться налетом окислов, приобретая пятна различных оттенков и радужные разводы.
Виды меднения
Процедура меднения доступна для выполнения даже новичками. Для этого достаточно только знать её основные тонкости. Существует два способа меднения в домашних условиях: с погружением в электролит и без погружения.
Метод погружения
В домашних условиях поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
Дальше:
- Анодную пластину (можно две) помещают в емкость, которую будем называть ванной. На аноды замыкают положительную клемму.
- Между анодами на любом удобном проводнике подвешивается деталь, к ней подводят отрицательный полюс от блока питания.
- Готовый раствор вливается в ванночку – при этом уровень покрытия должен быть выше, чем расположена деталь.
- После подключения электродов к источнику тока выставляют рабочий ток. Это примерно 1 А/кв.дм. покрытия.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Покрытие без погружения
Данный способ меднения имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшую толщину металла. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Порядок действий при гальваническом меднении в домашних условиях:
- Готовят «тампон» для нанесения покрытия. Берут медный проводник и наматывают кусок искусственной ткани (полиэстер подойдет).
- Противоположный конец проводника подсоединяют к положительной клемме источника напряжения.
- Электролитным раствором наполняют емкость – так удобнее окунать карандаш.
- Деталь аккуратно очищают и обезжиривают, а потом помещают в пустую ванночку. Там изделие подсоединяется к отрицательной клемме.
- Тампон смачивают в растворе. Затем им проводят по поверхности изделия, закрашивая ее постепенно.
Процесс длится до полного покрытия медным слоем изделия.
Необходимые инструменты для меднения в домашних условиях
«Ингредиенты», без которых меднение не состоится:
- Источник постоянного тока. Выбирается в зависимости от размера изделия.

- Аноды. Анодные пластины выполняют несколько функций. В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
- Рабочий электролит. Кислотный, щелочной или пирофосфорный раствор. Состав электролита выбирается в зависимости от исходного металла. Необходимо помнить, что любой электролит не универсален и подойдет не для всех работ.
Как подготовить простой электролит меднения
Стоит отметить, что гальваника в домашних условиях медью сложна, потому что химические реактивы найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
- Дистиллированная вода (или бидистиллят).
- Медный купорос.
- Соляная или другая кислота.

Готовый раствор имеет яркий синий цвет, запаха нет. Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами, особенно в домашних условиях: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах, а также обязательно указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.
Химическое меднение — это альтернатива электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды металла подвергаются очистке по-разному:
- Сталь.
 Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 °C. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 °C. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой. - Медь и сплавы. Обезжиривание осуществляется едким натрием, нагретым предварительно до 40°, около 10 минут.
- Чугун. Для процесса обезжиривания нужен раствор, содержащий едкий натрий, жидкое стекло, карбонат натрия и фосфат натрия при нагревании до 90°.
- Вольфрам. Меднение вольфрама в домашних условиях начинается с чистки предмета от грязи и прочих дефектов наждачной бумагой.
Техника безопасности при меднении в домашних условиях
Несмотря на возможность гальваники в домашних условиях (меднения), процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому нужно неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью в домашних условиях – работайте только в нежилом, хорошо проветриваемом помещении. Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты при меднении в домашних условиях нужно:
- Постоянно быть в респираторе, чтобы обезопасить дыхательные пути. лучше всего использовать вытяжку.
- Защитить руки прочными прорезиненными перчатками.
- Надеть специальную форму или клеенчатый фартук, противоожоговую обувь.
- Не забыть очки для безопасности зрительных органов.
- Не приносить в помещение еду и питье.
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Видео
В сюжете — Электролитическое омеднение в домашних условиях
В сюжете — Покрытие металлов медью в домашних условиях
В сюжете — Меднение на кухне
В продолжение темы посмотрите также наш обзор Удаление ржавчины с помощью пищевой соды
Источник
https://santekhnik-moskva. blogspot.com/2021/04/Kak-pokryt-sloyem-medi-metallicheskiye-izdeliya.html
blogspot.com/2021/04/Kak-pokryt-sloyem-medi-metallicheskiye-izdeliya.html
Меднение свинца в домашних условиях. Покрытие металла медью в домашних условиях
Содержание статьи:
Меднение в домашних условиях – это технологический процесс, позволяющий наносить на металл, а также другие материалы (вольфрам, сталь) слой меди толщиной от 1 до 300 мкм. Покрытие медным слоем обеспечивает хорошую адгезию металла и при увеличении толщины покрытий придает блеск изделиям, устраняет небольшие дефекты, позволяет создавать копии вещи. Удивительно, но все это можно делать и самим. Сегодня мы расскажем, как осуществить меднение металла в домашних условиях.
Гальваника медью в домашних условиях: общие сведения
С технической точки зрения обработка – это электрохимический процесс. В процессе всегда есть два «участника» анод+электролит (источник металла) и деталь.
Технология гальваники медью в домашних условиях достаточно проста. Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Среди основных этапов гальванического меднения в домашних условиях:
- Подготовка поверхности (механическая и химическая).
- Нанесение подслойного покрытия (если необходимо)
- Меднение в соответствующем исходному металлу электролите.
Для декоративного гальванического меднения подойдут электролиты матового и блестящего меднения. После нанесения слоя, можно обработать поверхность в электролитах серебра, золота никеля и т.д.
Необходимые инструменты для меднения в домашних условиях
«Ингредиенты», без которых меднение не состоится, но которые реально подготовить в домашних условиях. Наши гальваники утверждают, что прежде всего, нужны:
- Источник постоянного тока.Выбирается в зависимости от размера изделия.
- Аноды. Анодные пластины выполняют несколько функций.
 В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия. - Рабочий электролит. Кислотный, щелочной или пирофосфорный раствор. Состав электролита выбирается в зависимости от исходного металла. Необходимо помнить, что любой электролит не универсален и подойдет не для всех работ.
Подготовка материала
Как правильно подготовить простой электролит меднения
Стоит отметить, что гальваника в домашних условиях медью сложна, потому что химические реактивы найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
- Дистиллированная вода (или бидистиллят).
- Медный купорос.
- Соляная или другая кислота.
Готовый раствор имеет яркий синий цвет, запаха нет.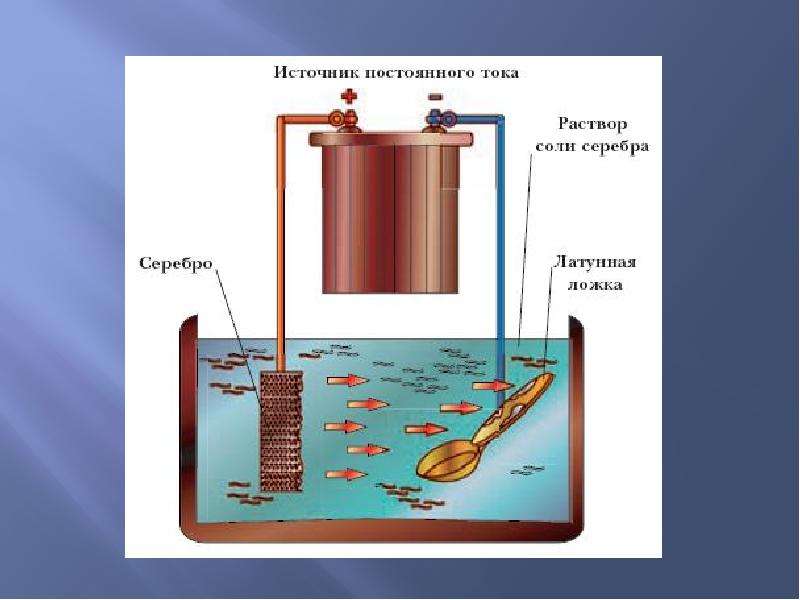 Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами, особенно в домашних условиях: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами, особенно в домашних условиях: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах, а также обязательно указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.
Подготовка материала для меднения в домашних условиях
Химическое меднение — это альтернатива электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды металла подвергаются очистке по-разному:
- Сталь.
 Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
- Медь и сплавы. Обезжиривание осуществляется едким натрием, нагретым предварительно до 40°, около 10 минут.
- Чугун. Для процесса обезжиривания нужен раствор, содержащий едкий натрий, жидкое стекло, карбонат натрия и фосфат натрия при нагревании до 90°.
- Вольфрам. Меднение вольфрама в домашних условиях начинается с чистки предмета от грязи и прочих дефектов наждачной бумагой.
Техника безопасности при меднении в домашних условиях
Несмотря на возможность гальваники в домашних условиях (меднения), процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому нужно неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью в домашних условиях – работайте только в нежилом, хорошо проветриваемом помещении.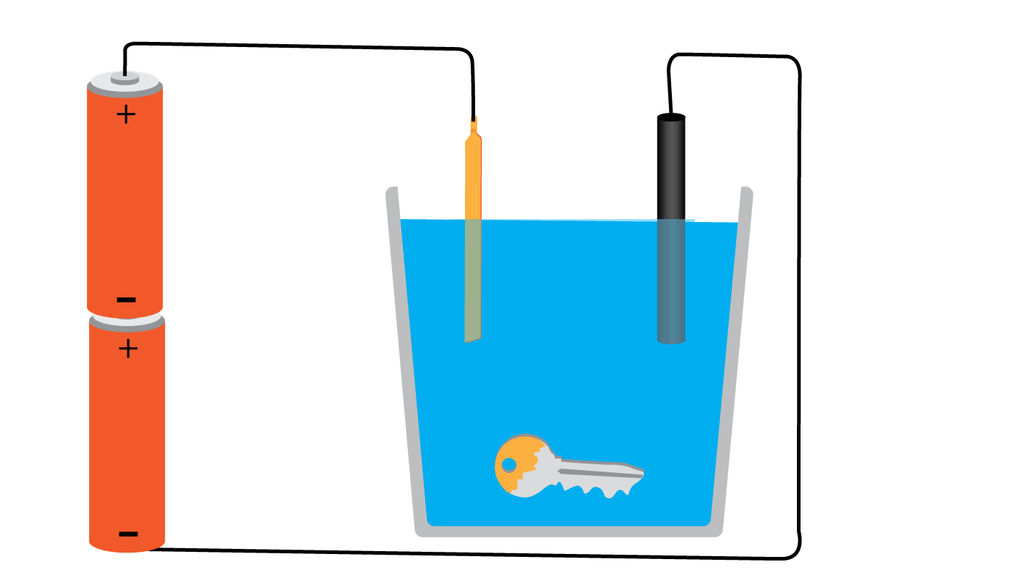 Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты при меднении в домашних условиях нужно:
- Постоянно быть в респираторе, чтобы обезопасить дыхательные пути. лучше всего использовать вытяжку.
- Защитить руки прочными прорезиненными перчатками.
- Надеть специальную форму или клеенчатый фартук, противоожоговую обувь.
- Не забыть очки для безопасности зрительных органов.
- Не приносить в помещение еду и питье.
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Гальваника в домашних условиях: меднение
Почему в гальванике столь востребована именно медь? Она имеет высокую адгезию (иными словами – сцепление) к самым разным материалам. Это значит, что она превосходно держится на изделиях из стали, вольфрама, не отлетая и не скалываясь.
Медь – красивый яркий металл, внешне напоминает самородки розово-красного оттенка. Материал проводит не только тепло, но и электрический ток – отсюда и высокий спрос в сфере электротехники и приборостроении. Однако чистую медь найти сложно. Чаще она поставляется с различными примесями.
Медные покрытия:
- Отличаются малым сопротивлением, что используется в электротехнике
- Скрывает мелкие недочеты поверхности.
- Быстро окисляется, что используют для получения эффекта «антик».
Технологий меднения существует две. Одна происходит путем погружения изделия в раствор электролиты (с подачей тока или без). Второй же способ – это метод селективного нанесения покрытия без погружения в раствор. Рассмотрим оба.
Метод погружения
В домашних условиях поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
- Анодную пластину (можно две) помещают в емкость, которую будем называть ванной.
 На аноды замыкают положительную клемму.
На аноды замыкают положительную клемму. - Между анодами на любом удобном проводнике подвешивается деталь, к ней подводят отрицательный полюс от блока питания.
- Готовый раствор вливается в ванночку – при этом уровень покрытия должен быть выше, чем расположена деталь.
- После подключения электродов к источнику тока выставляют рабочий ток. Это примерно 1 А/кв.дм. покрытия.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Покрытие без погружения
Данный способ меднения имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшую толщину металла. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Порядок действий при гальваническом меднении в домашних условиях:
- Готовят «тампон» для нанесения покрытия. Берут медный проводник и наматывают кусок искусственной ткани (полиэстер подойдет).
- Противоположный конец проводника подсоединяют к положительной клемме источника напряжения.

- Электролитным раствором наполняют емкость – так удобнее окунать карандаш.
- Деталь аккуратно очищают и обезжиривают, а потом помещают в пустую ванночку. Там изделие подсоединяется к отрицательной клемме.
- Тампон смачивают в растворе. Затем им проводят по поверхности изделия, закрашивая ее постепенно.
Процесс длится до полного покрытия медным слоем изделия.
Особенности гальванопластики в домашних условиях
Гальванопластика — это процесс нанесения меди на проводящую или непроводящую поверхность изделия с последующим снятием покрытия с негативной матрицы. Таким образом можно получить множество очень точных копий с одного изделия. При этом, есть условие: наращивание меди толщиной не менее 200 мкм, чтобы изделие получилось прочным.
Важно учесть, что, если поверхность изделия не имеет свойств проводника, то потребуется больше усилий – а именно, особое предварительное покрытие графитом, серебром или медью. Основным металлом для осуществления гальванопластики считается медь, но можно выращивать матрицы из серебра чистотой 9999.
Обучение гальванике
Можно сделать вывод, что меднение сегодня — это один из наиболее актуальных гальванотехнических процессов, обучиться которому может каждый. Компания «6 микрон» проводит обучение по направлению «Гальваника» для всех желающих! Вы сможете выбрать удобную для Вас программу обучения, которая лучше всего подойдет для гальваники в домашних условиях и не только. Все интересующие вопросы можно задать по телефону или по электронной почте, наши технологи проконсультируют по курсам для обучения.
Видео руководство по меднению деталей в домашних условиях:Основной задачей гальванического покрытия медью в домашних условиях или по-другому меднения является подготовка поверхности металла к его дальнейшей обработке. Такой операции могут подвергаться различные металлы, и не металлы, среди которых следует выделить:
- сталь,
- латунь,
- никель и другие.
Использование меди
Благодаря своим многочисленным преимуществам данный металл получил широкое распространение. На сегодняшний день медь и ее многочисленные сплавы широко используются в промышленности. Металл актуальный для авиастроения, автомобилестроения, приборостроения и других отраслей. Не меньшей популярностью металл и изделия из него пользуются и в бытовой сфере. Меднение само по себе является одним из лучших способов покрытия тонким слоем металлической поверхности. В домашних условиях меднение можно выполнить нескольким способами.
На сегодняшний день медь и ее многочисленные сплавы широко используются в промышленности. Металл актуальный для авиастроения, автомобилестроения, приборостроения и других отраслей. Не меньшей популярностью металл и изделия из него пользуются и в бытовой сфере. Меднение само по себе является одним из лучших способов покрытия тонким слоем металлической поверхности. В домашних условиях меднение можно выполнить нескольким способами.
Гальваническое меднение в домашних условиях
Для этого понадобится:
Гальваническое меднение в домашних условиях
Приготовления раствора
Делаем насыщенный раствор медного купороса, после чего нужно будет добавить 1/3 этого раствора в соляную кислоту. После приготовления раствора медного купороса его следует тщательно размешать, чтобы не было частиц. Далее нужно соляную кислоту тонкой струйкой добавить в этот раствор. Не следует забывать про технику безопасности и использовать перчатки и защитные очки. После того, как вы добавили в раствор соляную кислоту, его следует тщательно перемешать.
Итак, раствор готов и можно приступать к меднению в домашних условиях. Для этого нужно взять металлическую деталь, на которую вы собрались наносить слой меди и подготовить ее к работе. Подготовка включает в себя ее обработку наждачной бумагой. Данная процедура позволяет не только зачистить металлическую поверхность, но и обезжирить ее. Такая же процедура будет актуальна и для детали из латуни или свинца. После этого, покрытие нужно тщательно промыть в растворе кальцинированной соды. Это позволит более тщательно обезжирить материал.
Кальцинированная соды для обезжиривания материала
Далее поверхность нужно погрузить в раствор медного купороса и соляной кислоты. Следует обратить внимание на то, что первый слой меди является очень тонким и слабым, поэтому его желательно снять при помощи металлической щетки. После того, как вы это сделали, поверхность стали или свинца следует повторно промыть в растворе кальцинированной соды и опять погрузить в раствор для меднения. Данные манипуляции приведут к тому, что слой меди в домашних условиях на поверхности будет гораздо толще и гораздо крепче, поскольку его убрать можно будет с предмета, только используя наждачную бумагу, а не металлическую щетку как прошлый раз.
Данные манипуляции приведут к тому, что слой меди в домашних условиях на поверхности будет гораздо толще и гораздо крепче, поскольку его убрать можно будет с предмета, только используя наждачную бумагу, а не металлическую щетку как прошлый раз.
Этот способ позволяет сделать очень качественное медное покрытие, которое можно снять только наждачкой. Для улучшения медного покрытия в домашних условиях следует деталь еще раз погрузить в раствор. Указанный способ отличается своей простотой и высокой эффективностью в том числе и для изделий из свинца.
Процедура меднения
Меднением принято называть процедуру гальванического нанесения меди, толщина слоя меди в таких случаях может составлять-от 300 мкм и больше. Меднение стали это один из наиболее важных процессов в гальванике, поскольку используется, как дополнительный процесс перед нанесением других металлов для хромирования, никелирования, покрытие серебром.
Слой меди прекрасно держится на стали и способен выравнивать различные дефекты на поверхности.
Для медных покрытий характерно высокое сцепление с другими поверхностями, изделиями из свинца особенно металлическими, а также высокая электропроводность и пластичность. Нанесенное недавно покрытие имеет ярко-розовый матовый или же блестящий цвет. Под воздействием влияний атмосферы медные покрытия могут окисляться, покрываться налетом окислов с различными пятнами радужного вида.
Сферы использования омеднения
Как правило, гальваническое омеднение может использоваться:
- В декоративных целях. С учетом огромной популярности в нынешнее время старинных изделий из меди. Существуют методы искусственного состаривания изделий из стали;
- В гальванопластике. Широко распространена в ювелирной сфере, среди сувенирной продукции, для изготовления барельефов и т.д;
- В технической отрасли. Меднение металла очень важно в электротехнической области. Низкая стоимость меднения по сравнению с покрытиями из золота или серебра позволяет снизить расходы на изготовление электродов, электротехнических шин, контактов и других элементов из сталии свинца.

Меднение происходит вместе с нанесением других гальванических покрытий
- Если нужно нанести многослойное защитно-декоративное покрытие на слой стали. В подавляющем большинстве случаев здесь медь используют вместе с никелем и хромом. Это позволяет улучшить сцепление с основным металлом и получить блестящее покрытие высокой прочности;
- Во избежание цементации участка. Меднение свинца позволит избежать появления углероживания на стальных участках. Для нанесения медного слоя используют только те участки, на которых будет проводиться обработка резанием;
- При выполнении реставрационных и восстановительных работ. Данный метод наиболее часто используется для восстановления хромированных частей автомобилей и мотоциклов. Для этих целей наносится довольно толстый слой меди, порядка 100-250 мкм и более того, что позволяет закрыть все дефекты и повреждения металла для нанесения последующих покрытий;
Разновидности меднения
- Используя погружение в электролит;
- Без погружения в электролит.

Первый способ предполагает обработку металлического изделия наждачной бумагой, щеткой и промывки водой. После чего обезжиривания в горячем содовом растворе с повторной промывкой. Далее в стеклянную емкость опускают на медных проволочках две медные пластины –аноды. Между пластинками на проволоке подвешивают деталь, после чего пускается ток.
Второй способ актуальный для изделий из стали, алюминия и цинка.
Домашнее омеднение
Данная процедура актуальна для различных случаев, поскольку нанесение слоя меди может использоваться для алюминиевых столовых приборов, сувениров, подсвечников и т. д. Неповторимый эффект оказывают изделия не из металла, на которые был нанесен слой меди. Это могут быть стебли растений, листья и др. Ввиду того, что в покрываемых предметах отсутствует токопроводящий слой, вместо него используется специальный электропроводный лак, который наносят на поверхности.
В состав лака входит ряд органических растворителей, пенкообразователей и тонкодисперсионный графитовый порошок, благодаря которому создается электропроводность. Лак наносят тонким слоем на сухую поверхность, и после высыхания через час можно приступать к омеднению. При желании можно меди придавать различные цветовые оттенки, используя для этого специальные способы. Высокое качество и уникальность таких изделий вполне заслуженно приравнивается к настоящим ювелирным украшениям.
Лак наносят тонким слоем на сухую поверхность, и после высыхания через час можно приступать к омеднению. При желании можно меди придавать различные цветовые оттенки, используя для этого специальные способы. Высокое качество и уникальность таких изделий вполне заслуженно приравнивается к настоящим ювелирным украшениям.
Видео: Меднение в домашних условиях
Для того чтобы подготовить металлический предмет к дальнейшей обработке, его нужно покрыть медью — такой процесс называют гальваностегией. Принцип его действия заключается в осаждении на поверхность обрабатываемой детали из другого металла, который растворен подходящим средством. Из данной статьи вы узнаете, как покрыть медью металл в домашних условиях, чтобы реализовать все последующие свои задумки с заготовкой.
Для чего это нужно?
Технология гальваностегии включает в себя создание раствора и образование различных электродов. Во время этого процесса медные ионы, которые растворены в электролите, притягиваются минусовым полюсом обрабатываемой детали на свою поверхностную точку.
Гальваностегия металлических деталей в промышленности применяется не только как завершающий обрабатывающий процесс. Она может применяться для того, чтобы подготовить детали к последующей операции (к примеру, хромированию, никелированию, серебрению каких-либо предметов).
В домашних условиях чаще всего проводится химическое меднение деталей. Также стоит заметить, что есть множество способов проведения такой процедуры, каждый из которых имеет свои преимущества и недостатки.
Сферы использования гальваностегии
Покрывать медью металл в домашних условиях в последнее время стало очень полезно. Чаще всего к такой процедуре подходят в следующих целях:
- В декоративных. Например, таким способом состаривают различные детали для того, чтобы придать винтажный вид.
- В гальванопластике. Очень часто наносят медный слой на сувениры, ювелирные украшения.
- В отрасли техники. Это связано с низкой стоимостью омеднения.
- Для нанесения защитно-декоративной прослойки того или иного изделия.

- Для того чтобы реставрировать или восстанавливать какие-либо детали.
Гальваностегия электролитным раствором
Таким способом можно покрыть медью сталь в домашних условиях, а также другие детали за исключением алюминия и цинка.
Для дальнейшей процедуры необходимо подготовить следующие материалы:
- Небольшие пластины из меди.
- Токопроводящая проволока (лучше запастись несколькими метрами).
- Источник тока, напряжение которого не должно быть более, чем 6 В.
- Реостат, чтобы регулировать ток.
- Амперметр.
- Электролит.
Важно! Последний компонент можно приобрести в специальном магазине, а можно и изготовить самостоятельно. Для этого нужно сделать раствор серной кислоты и дистиллированной воды при соотношении 2/100 мл. Нужный раствор получится, когда вы добавите к составу не больше 20 г медного купороса.
Суть работы заключается в следующем:
- Очистить обрабатываемую деталь наждачной бумагой — это нужно для того, чтобы снять оксидную пленку.
 Далее покрыть медью металл в домашних условиях будет не так трудно.
Далее покрыть медью металл в домашних условиях будет не так трудно. - Обезжирить металлическим предмет горячим раствором соды, промыть его чистой водой.
- В подходящую по объему емкость из стекла налить приготовленный электролит.
- Опустить в жидкость две пластины из меди на подготовленных токопроводящих проводках. Между двумя пластинками из меди подвешивается уже обезжиренная деталь на таком же проводке.
Важно! Проследите за тем, чтобы пластины из меди были полность погружены в электролит.
- Далее концы проводов от пластин из меди присоединяются к положительной клемме источника тока, а деталь — к отрицательной. Далее в созданную электросеть нужно подключить амперметр с реостатом. После того, как ток подключится к цепи, реостатом нужно установить его примерно 15 мА на 1 см площади детальной поверхности.
- Далее деталь выдерживается примерно 15-20 минут.
- По истечении времени нужно отключить электропитание и вытащить обрабатываемый металл из раствора.

В конечном итоге вы заметите, что смогли покрыть медью металл в домашних условиях, ведь он полностью покроется тонкой блестящей пленкой.
Важно! Толщина медного слоя будет зависеть от того, как долго была выдержана деталь в электролите.
Гальваностегия другим способом
Данный способ отлично подойдет для металлов-исключений, что были названы ранее — цинка и алюминия.
Алгоритм работы:
- Вооружиться многожильным проводом из меди, снять изоляцию с обоих его концов.
- Растеребить мягкий провод с одной стороны, получив имитированную кисточку. Привязать к этому концу предмет, похожий на рукоятку.
- Противоположную сторону провода необходимо соединить к плюсовой клемме источника электротока.
Важно! Напряжение должно быть не более, чем 6 В.
- Подготовить электролит описанным выше способом, вылить его в широкую тару — это нужно для удобства макания туда “кисточки”.

- Положить внутрь подготовленной емкости небольшую деталь из металла. Соединить ее, используя при этом провод, к отрицательной клемме токового источника также с напряжением 6 В.
Важно! Деталь должна быть предварительно очищена и обезжирена.
- Процесс покрытия алюминия медью в домашних условиях заключается в следующем: кистообразный конец провода нужно промакивать электролитным раствором и проводить им по поверхности обрабатываемого металлического предмета, не касаясь его. Дальше — отрицательно заряженный металл притянет к себе медные ионы и ее поверхность приобретет медную пленку.
Важно! Следите за тем, чтобы между концом растеребленной проволоки и металла был маленький слой электролитного раствора (и катод, и анод обязательно должны быть смочены этим раствором).
Гальваника представляет собой раздел электрохимической науки, которая изучает осаждение некоторых элементов на любую поверхность. С помощью гальваники в домашних условиях или в промышленности можно нанести на изделие тонкий слой металла, который будет выступать в роли защитного слоя или выполнять декоративные функции. В последнее время декоративное покрытие набирает популярность у тех, кто хочет сделать оригинальный подарок своим друзьям и родным.
С помощью гальваники в домашних условиях или в промышленности можно нанести на изделие тонкий слой металла, который будет выступать в роли защитного слоя или выполнять декоративные функции. В последнее время декоративное покрытие набирает популярность у тех, кто хочет сделать оригинальный подарок своим друзьям и родным.
Общие сведения
Покрытие гальваникой бывает технологическим или декоративно-защитным. Это тонкий металлический тонкий слой, который в зависимости от гальванических элементов может выполнять эстетические функции. Гальванопластика не увеличивает прочность изделия, поскольку в этом случае требуются большие производственные мощности, но для красоты и придания «свежести» вполне подойдет.
Гальванические реакции происходят с помощью постоянного электрического тока. В специальную емкость-диэлектрик наливают раствор — электролит, в который погружают два анода. Аноды должны быть изготовлены из металла, который будет осаждаться на покрываемом изделии.
Обрабатываемая деталь присоединяется к минусовому выводу и помещается между анодами. Она выполняет роль катода. Аноды, в свою очередь, присоединяются к плюсовому контакту источника питания. Они становятся частью цепи, проводя ток в электролит и отдавая ему свои металлические элементы. Электролит передает необходимые частицы обрабатываемой детали, они постепенно обволакивают её тонким слоем. Аноды по площади должны превышать в несколько раз размер заготовки.
Другими словами, гальванизация представляет собой перенос молекул металла раствора на изделие в момент протекания через них электротока.
Любой гальванический процесс можно разбить на общие этапы:
- Сборка гальванической установки.
- Подготовка электролитного раствора.
- Обработка и подготовка образца.
- Запуск гальванического процесса.
Оборудование можно подготовить самостоятельно. Сначала подбирается подходящий источник питания. Это может быть батарейка (для обработки изделий небольшого размера) или аккумулятор. Подойдет понижающий блок питания, который выдает на выходе постоянный ток до 12 вольт. Иногда используют инвертор от сварочного аппарата. Подбирается реостат для регулирования силы тока.
Подойдет понижающий блок питания, который выдает на выходе постоянный ток до 12 вольт. Иногда используют инвертор от сварочного аппарата. Подбирается реостат для регулирования силы тока.
Из нейтрального, устойчивого к химически агрессивным веществам материала подбирается широкая и глубокая ванночка. Надо учитывать, что электролитический раствор при гальваническом процессе может нагреваться до девяноста градусов по Цельсию.
Подготавливаются две пластины, которые будут токопроводящими анодами.
Для нагрева ёмкости с электролитом нужен электрический прибор с возможностью плавной регулировки температурного режима. Чаще всего используют подошву утюга или небольшую электроплитку. С их помощью происходит нагрев раствора до необходимой температуры и ускорение реакции.
Химические реактивы необходимо хранить в плотно закупоренной стеклянной посуде. Желательно каждый предмет подписывать.
Потребуются весы для точного измерения массы веществ, поскольку необходимая точность веса компонентов составляет один грамм. Такие весы можно приобрести, а можно сделать самостоятельно, используя вместо гирек старые советские монеты. Вес «желтых» монет точно соответствует их номиналу.
Такие весы можно приобрести, а можно сделать самостоятельно, используя вместо гирек старые советские монеты. Вес «желтых» монет точно соответствует их номиналу.
После того как собраны необходимые вещества, найдены ёмкости, собрана электрическая схема с питанием и подготовлена система подогрева, можно заняться чисткой заготовки.
Если недостаточно хорошо почистить деталь, гальваническое покрытие непрочно осядет или будет неравномерным. Иногда хватает простого обезжиривания предмета. Раствор ацетона или спирта может хорошо обезжирить поверхность, можно использовать бензин.
Некоторые мастера держат изделия из стали в разогретом до 90 градусов по Цельсию растворе фосфорнокислого натрия. Цветные металлы можно очищать в том же растворе, не нагревая его.
Если на изделии есть коррозия или другие изъяны, то поверхность заготовки шлифуется наждачной бумагой.
Иногда про технику безопасности при различных работах в домашних условиях рассказывают вскользь. Но при выполнении любых гальванических работ нужно строго соблюдать безопасность.
Но при выполнении любых гальванических работ нужно строго соблюдать безопасность.
Опасность заключается в использовании токсичных химических веществ, высокой температуре нагрева раствора и повышенными рисками, которые сопровождают электрохимические реакции.
Лучше всего гальванические работы проводить в гараже или мастерской при обязательном проветривании или вентилировании помещения. Особое внимание следует уделить заземлению оборудования. Нужно соблюдать меры личной безопасности, а именно:
- Дыхательные пути следует защитить респиратором.
- Руки и запястья должны быть спрятаны в высокие и прочные резиновые перчатки.
- Обувь должна защищать от ожогов, а одежда прикрыта клеенчатым фартуком.
- Обязательно ношение специальных защитных очков.
Перед началом работ по меднению в домашних условиях нужно подготовить необходимые материалы и оборудование. Надо позаботится об источнике напряжения и постоянного тока. Существует много рекомендаций касательно силы тока, разброс которого может быть большим. Поэтому желательно иметь реостат с возможностью плавной регулировки напряжения и для постепенного завершения процесса. Источником может служить автомобильный аккумулятор или выпрямитель с напряжением на выходе не больше 12 вольт. Для первых опытов будет достаточно обычной батарейки от 4.5 до 9 вольт.
Поэтому желательно иметь реостат с возможностью плавной регулировки напряжения и для постепенного завершения процесса. Источником может служить автомобильный аккумулятор или выпрямитель с напряжением на выходе не больше 12 вольт. Для первых опытов будет достаточно обычной батарейки от 4.5 до 9 вольт.
Затем выбирается ёмкость для электролитического раствора, лучше всего из жаропрочного стекла. В любом случае все ёмкости для электролиза должны быть диэлектриками и выдерживать температуру не менее, чем 80 градусов по Цельсию.
В качестве анодов подойдут два больших медных листа. Они должны перекрывать по размеру заготовку. Из химических реактивов потребуются:
- Купорос медный.
- Кислота соляная либо серная.
- Вода дистиллированная.
Меднение в домашних условиях пользуется заслуженной популярностью, поскольку очень хорошо и надежно держится на стальных изделиях. Главное условие — правильно соблюдать технологию процесса.
Имеется два способа нанесения меди на поверхность:
- Помещение заготовки в раствор электролита.

- Неконтактный способ. В этом случае изделие не погружается в раствор.
Подготавливается и обрабатывается поверхность изделия при помощи тонкого наждака и щеточки. После этого деталь моется в проточной воде, обезжиривается и еще раз промывается.
Этапы процесса омеднения следующие:
- Два медных анода подключают в сеть к положительным контактам и размещают их в стеклянную банку.
- К обработанному изделию подводят контакт с отрицательным значением напряжения и свободно подвешивают между анодами.
- Подключают реостат согласно электрической схеме для возможности регулирования силы тока.
- Подготавливается раствор в правильных пропорциях. На 100 г дистиллированной воды надо 20 г медного купороса и 2−3 г соляной кислоты. Вместо соляной кислоты можно использовать другую.
- Раствор выливается в посуду с медными пластинами и деталью таким образом, чтобы они полностью скрылись под поверхностью раствора.
- Подключается источник напряжения.
 Реостатом добиваются необходимой силы тока из примерного расчета 10−15 миллиампер на каждый квадратный сантиметр площади детали.
Реостатом добиваются необходимой силы тока из примерного расчета 10−15 миллиампер на каждый квадратный сантиметр площади детали.
Весь процесс занимает примерно 15−20 минут. После обязательного выключения источника питания и остывания раствора готовое изделие с медным слоем на поверхности вынимается из банки.
Этот метод интересен тем, что его можно использовать для обработки не только стальных предметов, но и сделанных из других материалов. Например, алюминия и цинка. Порядок процесса следующий:
- Из многожильного медного провода изготавливается «кисточка». Конец провода оголяется. Из медных проводков создается подобие кисточки, чтобы затем прикрепить ее к деревянной ручке-держателю.
- Второй конец провода подключается к плюсовому контакту электрической цепи.
- В широкую ёмкость заливается стандартный электролитный раствор из медного купороса и соляной кислоты.
- Предварительно очищенная и промытая металлическая заготовка присоединяется к отрицательному контакту и размещается в пустой ёмкости.

- Импровизированная кисточка окунается в раствор электролита и проводится по поверхности заготовки без контакта. Это действие повторяется до получения результата.
Когда деталь полностью покроется слоем меди, выключается блок питания и процесс завершается. Деталь ополаскивается в воде и просушивается.
Часто с помощью медного электролиза обновляют столовые приборы, сделанные из алюминия. Если нет опыта проведения этого процесса, то можно потренироваться нанести медь на алюминиевые пластинки. Порядок проведения процесса:
Гальванопластика — это электрохимический способ придания предмету определенной формы с помощью осаждения на него металла. Чаще всего этот метод используют при обработке металлом неметаллических предметов или при изготовлении копий ювелирных изделий.
Если при гальванопластике изделие не обладает электропроводящими свойствами, то его предварительно покрывают графитом, иногда бронзой. Затем мастер делает с копии слепок и начинает гальванический процесс. В качестве материала слепка используют гипс, графит или легко плавящийся металл.
В качестве материала слепка используют гипс, графит или легко плавящийся металл.
Гальваника — это очень интересный и познавательный процесс, но он связан с активными веществами, которые могут навредить здоровью и нанести вред имуществу или окружающей среде. Поэтому перед тем как начинать гальванику своими руками, нужно принять все меры безопасности, изучить немного теории процесса и особенности поведения химических реактивов.
Медь — это один из древних металлов: люди начали применять ее для создания орудий труда еще в 4 тысячелетии до нашей эры. Такое широкое распространение меди объяснимо тем, что вещество встречается в природе в металлическом самородном состоянии. И сегодня медь используется повсеместно — в металлургии, автомобильной промышленности, электротехнике и строительстве.
Состав меди
Металлическая медь представляет собой тяжелый металл розово-красного цвета, ковкий и мягкий, который плавится при температуре больше 1080 градусов по Цельсию, очень хорошо проводит теплоту и электрический ток: электропроводимость меди выше в 1,7 раза, чем алюминия и больше в 6 раз выше, чем железа, и только немного уступает электропроводимости серебра.
Специфические особенности меди определяются содержанием в металле конкретных примесей, количество которых может различаться приблизительно в 10 — 50 раз. По содержанию кислорода принято использовать следующую классификацию меди:
- бескислородная медь с содержанием кислорода меньше 0,001%;
- медь рафинированная с содержанием кислорода от 0,001до 0,01%, но с увеличенным присутствием фосфора;
- медь большой чистоты с содержанием кислорода примерно 0,03-0,05%;
- металл общего назначения с содержанием кислорода 0,05 — 0,08%.
В меди кроме кислорода может присутствовать водород, который в металл попадает в процессе электролиза или при совершении отжига в атмосфере, которая содержит водяной пар. При высокой температуре водяной пар разлагается с формированием водорода, который в медь легко диффундирует.
Атомы водорода в бескислородной меди размещаются в междоузлиях кристаллической решетки и на свойствах металла особо не сказываются. В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с закисью меди, при этом образуется в толще меди водяной пар, которому присуще высокое давление, что приводит к вздутиям, трещинам и разрывам. Это явление носит название «водородная болезнь».
В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с закисью меди, при этом образуется в толще меди водяной пар, которому присуще высокое давление, что приводит к вздутиям, трещинам и разрывам. Это явление носит название «водородная болезнь».
Железо, висмут, сурьма и свинец ухудшают пластичность меди. Примеси, что являются малорастворимыми в меди (свинец, кислород, сера, висмут), провоцируют хрупкость при высокой температуре, что затрудняет процесс горячей обработки давлением.
Физические свойства меди
Основное свойство меди, определяемое её использование, — высокая электропроводность или малое удельное электрическое сопротивление. Подобные примеси как железо, фосфор, мышьяк, олово и сурьма, значительно ухудшают её электрическую проводность. На величину электропроводности оказывает большое влияние механическое состояние меди.
Второе важное свойство меди — значительная теплопроводность. Легирующие добавки и свойства уменьшают теплопроводность меди, поэтому созданные на медной основе сплавы самой меди значительно уступают по этому показателю.
Медь при нормальных температурах является коррозиционно устойчивой в таких средах, как пресная вода, сухой воздух, морская вода при небольшой скорости движения воды, неокислительные кислоты и растворы соли при отсутствии кислорода, сухие галогенные газы, щелочные растворы за исключением солей аммония и аммиака, органические кислоты, фенольные смолы и спирты.
В аммиаке, хлористом аммонию, окислительных минеральных кислотах и растворах кислых солей медь не устойчива. Её коррозионные свойства также заметно ухудшаются в некоторых средах с возрастанием количества примесей. Допускается контакт меди с её сплавами, с оловом, свинцом во влажной атмосфере, морской и пресной воде. В то же время контакт меди с цинком и алюминием не допускается вследствие их быстрого разрушения.
Медь, ее сплавы и соединения нашли широкое применение в разных отраслях промышленности. Медь в электротехнике используют в чистом виде в производстве шин контактного и голого проводов, кабельных изделий, электрогенераторов, телефонного оборудования и радиоаппаратуры. Из меди изготавливают вакуум-аппараты, теплообменники и трубопроводы.
Из меди изготавливают вакуум-аппараты, теплообменники и трубопроводы.
Сплавы меди с различными металлами используют в автомобильной промышленности и для изготовления химических аппаратов. Проволока из красной меди изготовления всевозможных шнуров и выгибания самых сложных элементов. Высокие свойства меди делают ее незаменимой при производстве филигранных деталей.
Процедура меднения
Меднением называют процедуру гальванического нанесения меди, толщина слоя которой составляет 1 — 300 мкм и больше. Меднение стали является одним из важнейших процессов в гальванике, что применяется в качестве предварительного процесса при подготовке металлической поверхности для покрытия другими металлами — при хромировании, никелировании и покрытии серебром, а также как законченный самостоятельный процесс.
Использование меднения как подготовительной манипуляции связано с тем, что этот металл способен очень прочно держатся на стали, выравнивать дефекты поверхности. Другие материалы на медь хорошо осаждаются, а вот на чистую сталь — не очень.
Медные покрытия характеризуются высоким сцеплением с разными металлами, высокой электропроводностью и пластичностью. Их принято наносить на стальные, цинковые и алюминиевые детали.
Только что нанесённое покрытие меди имеет ярко-розовый матовый или блестящий цвет, зависимо от технологии нанесения. Медные покрытия в атмосферных условиях способны легко окисляться и покрываться налетом окислов, приобретая пятна различных оттенков и радужные разводы.
Использование меднения
В большинстве своем гальваническое меднение металлов используют в таких случаях:
- В декоративных целях. Огромной популярностью в настоящее время пользуются старинные изделия из меди. Процедура меднения позволяет наносить на металл медные покрытия, которые как бы «состариваются» после специальной обработки и выглядят так, будто изготовлены давным-давно.
- В гальванопластике. Используется гальваническое меднение железа для создания металлических копий изделий разной формы и различных размеров.
 Создаётся пластиковая или восковая основа, которую покрывают электропроводящим лаком и слоем меди. Подобную технологию меднения часто используют при изготовлении ювелирных изделий, сувениров, барельефов, матриц и волноводов.
Создаётся пластиковая или восковая основа, которую покрывают электропроводящим лаком и слоем меди. Подобную технологию меднения часто используют при изготовлении ювелирных изделий, сувениров, барельефов, матриц и волноводов. - В технических целях. Меднение металла большое значение имеет в электротехнической области. Благодаря низкой стоимости меднения по сравнению с покрытиями золотом или серебром, медные покрытия нашли применение при изготовлении электротехнических шин, электродов, контактов и прочих элементов, которые работают под напряжением. Меднение зачастую используется как покрытие под пайку.
Меднение применяется в сочетании с прочими гальваническими покрытиями:
- При нанесении многослойного защитно-декоративного покрытия. Как правило, медь используется в сочетании с хромом и никелем (3-слойное защитно-декоративное покрытие) и прочими металлами как промежуточный слой для увеличения сцепления с основным металлом и получения более прочного и блестящего покрытия.

- Для предохранения участка при цементации. Меднение свинца способно предохранять участки стальных изделий от цементации — науглероживания. Покрывают медью исключительно те участки, которые подлежат в будущем обработке резанием. Твёрдый науглероженный поверхностный слой не поддается подобным обработкам, а медь может защитить покрытые участки от процесса диффузии углерода в них.
- При восстановлении и ремонте деталей. Меднение металла является важной процедурой при работах реставрационного характера и восстановлении хромированных частей мотто- и автомобильной техники. Наносить принято значительный слой меди — порядка 100-250 мкм и больше, который закрывает дефекты металла и поры и выполняет функции новой основы для последующих покрытий.
Виды меднения
Процедура меднения своими руками доступна для выполнения даже новичками. Для этого достаточно только знать её основные тонкости. Существует два способа меднения в домашних условиях: с погружением в электролит и без погружения.
С погружением в электролит
Металлическое изделие обрабатывают наждачной бумагой для удаления оксидной пленки, протирают щеткой, промывают как следует водой, обезжиривают в горячем содовом растворе и промывают еще один раз. После этого принято опускать в стакан или банку на медных проволочках две медные пластинки, которые являются анодами.
Между пластинками подвешивают на проволочке деталь. Проволочки, идущие от медных пластинок, соединяют вместе и подключают к плюсу источника тока, а деталь — к минусу. После этого в цепь включается реостат для регулировки тока и миллиамперметр. Необходим источник постоянного тока, который имеет напряжение не больше 6 В.
Для меднения дома нужно приготовить следующий раствор электролита. Возьмите 20 грамм медного купороса и 2-3 миллилитра серной кислоты на 100 миллилитров воды и налейте в посуду. Следите, чтобы данный раствор полностью покрыл электроды.
При использовании реостата нужно установить ток в пределах 10 — 15 мА на каждый сантиметр квадратный поверхности детали. Где-то через 20 минут следует выключить ток и вынуть изделие, оно уже покрылось тонким медным слоем. Чем дольше будет идти процесс, тем слой меди получится толще.
Где-то через 20 минут следует выключить ток и вынуть изделие, оно уже покрылось тонким медным слоем. Чем дольше будет идти процесс, тем слой меди получится толще.
Без погружения в электролит
Данную процедуру проводят для стали, алюминия и цинка. С одного конца многожильного провода снимают изоляцию, затем необходимо растеребить тонкие медные проволочки для получения медной кисти. Для удобства работы необходимо привязать ее к медной кисти или деревянной палочке, а другой конец кабеля нужно подсоединить к плюсу источника тока.
Дальше следует приготовить электролит — раствор медного купороса, лучше слегка подкисленный, и налить в широкую склянку, в которую кисть будет удобно макать. Подготовьте металлическую пластинку или какой-то другой маленький предмет с плоской поверхностью. Его нужно протереть с помощью мелкой наждачной шкурки и обезжирить посредством кипячения в растворе стиральной соды.
Затем необходимо положить пластинку в кювету или ванночку и подсоединить ее с помощью провода к минусу источника тока. После того, как схема собрана, вам следует только ввести электролит. Обмакните в раствор медного купороса «кисть», которой следует провести вдоль пластинки, не дотрагиваться до поверхности.
После того, как схема собрана, вам следует только ввести электролит. Обмакните в раствор медного купороса «кисть», которой следует провести вдоль пластинки, не дотрагиваться до поверхности.
Рекомендуется работать так, чтобы между кистью и пластинкой всегда располагался слой электролита. Все время работы проводки должны быть смоченными раствором. Пластинка на глазах будет покрываться слоем металлической меди красного цвета. Для обработки маленькой детали понадобятся считанные минуты.
Когда вы нанесли покрытие, нужно высушить на воздухе деталь и натереть матовый слой меди до блеска с помощью суконной или шерстяной тряпки. Процесс меднения алюминия, когда изделие в электролитическую ванну не опускают, а обрабатывают небольшими участками снаружи, добавляя электролит, применяют в таких случаях, когда изделие настолько велико, что для него нельзя подобрать подходящую ванны.
Ванны меднения
Установки для меднения от обыкновенных гальванических ванн ничем не отличаются. Электролиты для меднения довольно просто получить, если иметь под рукой необходимые ингредиенты. Бывают два вида медных растворов: щелочные и кислые.
Электролиты для меднения довольно просто получить, если иметь под рукой необходимые ингредиенты. Бывают два вида медных растворов: щелочные и кислые.
В кислых растворах вы не сможете получить хорошо сцепленные покрытия из меди на цинковых и стальных изделиях, потому что цинк и железо в этом случае растворяются с медью, и нарушается сцепление с защитным покрытием.
Для устранения данной особенности рекомендуется первый тонкий медный слой (2—3 мкм) создать в щелочном растворе для меднения, а в будущем наращивать покрытие до заданной толщины в кислом электролите, который является более экономичным. Цинковые изделия, что имеют сложную форму, лучше всего меднить в щелочных электролитах.
Самыми распространенными кислыми электролитами являются борфтористоводородные и сернокислые. Наибольшее использование нашли сернокислые электролиты, которые отличаются простотой состава, высоким выходом по току и значительной устойчивостью.
Перед меднением деталей из стали в кислых электролитах их рекомендуется предварительно меднить в цианистом электролите или осаждать тонкий подслой никеля. Данные электролиты имеют несколько недостатков.
Данные электролиты имеют несколько недостатков.
Один из них состоит в невозможности непосредственного покрытия цинковых и стальных деталей из-за контактного выделения меди, которая имеет плохое сцепление с металлом основы. Также электролиты незначительную рассеивающую способность и более грубую структуру осадков по сравнению с прочими электролитами.
Среди щелочных электролитов меднения известны пирофосфатные и цианистые электролиты.
Цианистые электролиты из меди характеризуются высокими рассеивающими способностями, возможностью проведения меднения столярных изделий и мелкокристаллической структурой осадков.
К недостаткам щелочных электролитов относят низкую плотность тока и неустойчивость раствора вследствие карбонизации под действием двуокиси углерода свободного цианида. Помимо этого, цианистые электролиты отличаются уменьшенным выходом по току — не больше 60-70%.
Таким образом, медь является металлом, который используется повсеместно: в автомобильной промышленности, электротехнике и строительстве. А в гальванопластике известна технология меднения для подготовки металлической поверхности под покрытие другими металлами или как самостоятельный процесс.
А в гальванопластике известна технология меднения для подготовки металлической поверхности под покрытие другими металлами или как самостоятельный процесс.
Гальваническое покрытие медью в домашних условиях. Покрытие металла медью в домашних условиях
Освоить технологию гальванического покрытия металлами материалов можно довольно быстро, для этого не потребуются обширные познания в физике или химии, а вот представление о том, что вы хотите получить «на выходе» — все же желательно иметь:)
Сам принцип омеднения заключается в осаждении меди на поверхности предмета-основы с помощью электро-химической обработки формы-полуфабриката.
По большому счету, доступный способ покрытия форм медью — всего один.
Технология омеднения различных неметаллических предметов называется «гальванопластика» («электроформинг» — западный аналог названия). Гальванопластическим способом вполне возможно изготовить самые разнообразные детали украшений.
Необходимым условием получения качественного медного покрытия является точное соблюдение технологии меднения. Итак, перейдем к созданию установки для омеднения.
Итак, перейдем к созданию установки для омеднения.
Омеднение (меднение) производят в емкостях, имеющих обычно округлую или прямоугольную форму. Другая форма емкости так же не помешает процессу. Объем емкости определяется размером и количеством изделий (предметов), подлежащих меднению. Вполне подходят глазурованные емкости из керамики, стекла или пластмассы .
Вам понадобится источник постоянного тока низкого напряжения (от 2 до 6В). Для этого идеально подходит выпрямители для зарядки аккумуляторов, а если такового в вашем хозяйстве не обнаружилось, то сойдут и аккумуляторные батареи или элементы питания (батарейки).
Силу тока регулировать можно с помощью ползункового реостата (не пугайтесь, его можно заметить подходящим переменным резистором, это выглядит как регулятор громкости, такая ручка или бегунок).
Так же понадобится мультиметр для контроля силы тока (от 0 до 3-5 ампер) и для измерения напряжения. Как правило, амперметр на зарядных устройствах все же присутствует и отдельно его приобретать не нужно.
Для создания электролита запаситесь медным купоросом и серной кислотой . Вместо серной кислоты прекрасно подходит электролит, которым обычно заправляют аккумуляторы для автомобилей.
Для нанесения токопроводящего слоя на поверхность детали, подлежащей омеднению, потребуется токопроводящий лак .
В качестве анода можно использовать медные пластины , а за неимением таковых — обычную медную проволоку — жилу, добытую из обычного силового кабеля, который можно купить в любом магазине электротехнических товаров. Площадь этой пластины или проволоки должна быть примерно равна площади покрываемого медью предмета, в любом случае — чем она больше, тем лучше. Задача анода — потихоньку растворяться, отдавая медь в раствор .
Еще для омеднения необходим будет этиловый спирт .
Электролит приготавливается следующим образом :
на 1 литр воды берется 230-250 грамм медного купороса и 40-50 мл. серной кислоты (серную кислоту можно приобрести в виде состава с названием «Электролит» в авто и хозяйственных магазинах).
серной кислоты (серную кислоту можно приобрести в виде состава с названием «Электролит» в авто и хозяйственных магазинах).
* Будьте осторожны при обращении с электролитом — он может повредить кожу, глаза и даже ткань одежды.
* Следует помнить, хотя растворы не содержат сильно ядовитых веществ, но обращаться с ними все же следует с определенной осторожностью, чтобы не получить отравление или ожог.
* Растворы целесообразно хранить в темной стеклянной емкости с хорошо закрывающейся крышкой (но прекрасно подойдет и обычная пластиковая бутылка).
Обработка поверхности различных предметов производится для придания декоративного эффекта или в качестве промежуточной процедуры, предваряющей дальнейшие действия. Многие процессы доступны для выполнения и не требуют большого количества оборудования. Один из наиболее популярных способов обработки — меднение, его можно выполнить и в домашних условиях.
Что представляет собой процесс меднения
Меднение — это процесс нанесения на поверхность предмета тонкого слоя меди. Оно выполняется гальваническим методом, т. е. путем переноса ионов меди от положительно заряженного источника на обрабатываемую поверхность, заряженную отрицательно. Чаще всего процесс гальванического нанесения меди является подготовительным этапом перед покрытием никелем и хромом, но нередко меднение металла становится самостоятельным видом финишной отделки. Широко используется гальванопластика, для которой требуется создать покрытие из меди.
Оно выполняется гальваническим методом, т. е. путем переноса ионов меди от положительно заряженного источника на обрабатываемую поверхность, заряженную отрицательно. Чаще всего процесс гальванического нанесения меди является подготовительным этапом перед покрытием никелем и хромом, но нередко меднение металла становится самостоятельным видом финишной отделки. Широко используется гальванопластика, для которой требуется создать покрытие из меди.
Разновидности меднения
Существует два варианта меднения в домашних условиях:
- С погружением обрабатываемой детали в электролит.
- Без погружения.
С погружением обрабатываемой детали в электролит. Для выполнения процедуры надо иметь емкость с электролитом, имеющую достаточный объем. После предварительной подготовки, состоящей в очистке поверхности наждачной бумагой и промывке в горячем растворе соды, предмет подключается к отрицательному электроду и погружается в электролит на определенное время.
Без погружения. Можно обработать сталь, алюминий, свинец, цинк. Обработка производится без погружения в емкость, обычно такой вариант применяется для крупных деталей.
Оба варианта вполне доступны для самостоятельного выполнения в домашних условиях.
Оборудование и материалы, необходимые для нанесения медного покрытия
Чтобы выполнять меднение стали или других металлов, придется запастись кое-какими материалами и устройствами. Понадобятся:
- Медный купорос (сернокислая медь).
- Источник постоянного тока, желательно с регулируемым напряжением (один из вариантов — ЛАТР), но подойдет и обычный трансформатор на 6–12 В.
- Емкость для электролита (оптимально — стеклянный резервуар).
- Две медных пластины, которые могут свободно поместиться в емкость.
Из воды, медного купороса и соляной кислоты надо изготовить электролит. Сначала в воду добавляется медный купорос, до получения насыщенного раствора. Его надо тщательно перемешивать, чтобы не оставалось твердых частиц. Затем в раствор тонкой струйкой добавляется соляная кислота (не наоборот!). Всего для нанесения покрытия понадобится:
Его надо тщательно перемешивать, чтобы не оставалось твердых частиц. Затем в раствор тонкой струйкой добавляется соляная кислота (не наоборот!). Всего для нанесения покрытия понадобится:
- — 980 г.
- — 190 г.
- — 40 г.
Теперь все готово, можно приступать к меднению в домашних условиях.
Внимание! Необходимо учитывать, что соляная кислота — химически активный реагент, поэтому следует запастись средствами защиты — перчатками, очками, максимально подготовить рабочее место.
Технология меднения
Порядок действий при нанесении покрытия:
- Надо удалить тонкую пленку окислов с поверхности детали, подлежащей обработке. Используется наждачная бумага, металлическая щетка или иные абразивные материалы. Необходимо действовать очень аккуратно, поскольку сильные повреждения металла останутся заметными. В идеале, поверхность должна быть отполирована.
- Затем изделие тщательно промывается в горячем растворе кальцинированной соды.
 Это действие позволяет обезжирить поверхность.
Это действие позволяет обезжирить поверхность. - Подготовленное изделие подключается к отрицательному электроду от источника питания и помещается в раствор электролита.
- В раствор электролита опускаются медные пластины с присоединенным к ним положительным электродом от источника питания (анод). Необходимо следить, чтобы анод и катод не соприкасались. В идеале, расстояние между ними должно быть во всех участках одинаковым, но на практике этого сложно добиться.
- Меднение металла производится в несколько приемов. Первый слой покрытия, полученный в течение нескольких минут, рекомендуется удалить и вновь промыть деталь в содовом растворе. Это усилит сцепление слоя омеднения с основным металлом. Деталь выдерживается в растворе около 20–30 минут. Толщина слоя покрытия может достигать 300 мкм.
Нередко бывает необходимо удалить слой покрытия с хромированных частей. Для этого на деталь подается отрицательный заряд, а на положительный электрод наматывается тряпочка, смоченная в растворе серной кислоты (5%). Ею протирается поверхность детали, слой хромирования снимается. При выполнении процедуры необходимо защищать кожу, органы зрения и дыхания от паров кислоты.
Ею протирается поверхность детали, слой хромирования снимается. При выполнении процедуры необходимо защищать кожу, органы зрения и дыхания от паров кислоты.
Меднение деталей без погружения в раствор
Гальваническое омеднение может выполняться без погружения детали в емкость с электролитом. Для этого надо подключить к ней отрицательный электрод. В качестве положительного контакта берется медный многожильный провод, конец которого освобождается от изоляции на 1–2 см и разминается так, чтобы получилось некое подобие кисти.
Для нанесения слоя медного покрытия «кисточка» обмакивается в электролит, затем ее концом проводят по поверхности детали, не прикасаясь к ней, но стараясь, чтобы между ними находилась прослойка. Постоянно обмакивая анод в электролит, покрывают слоем меди всю поверхность. Процедура требует навыка и времени, но результат того стоит.
Гальванопластика
Покрытие медью может быть выполнено не только на металлических предметах. Широко распространена гальванопластика, когда меднение выполняется по различным засушенным растениям, насекомым и прочим неметаллическим предметам.
Широко распространена гальванопластика, когда меднение выполняется по различным засушенным растениям, насекомым и прочим неметаллическим предметам.
Технология нанесения покрытия мало отличается от обычной, только вначале процесса на поверхность надо нанести электропроводный лак. После засыхания лакового покрытия производятся обычные действия по нанесению слоя меди. Полученные изделия обладают высокими декоративными или художественными качествами и высоко оцениваются зрителями.
Для того чтобы подготовить металлический предмет к дальнейшей обработке, его нужно покрыть медью — такой процесс называют гальваностегией. Принцип его действия заключается в осаждении на поверхность обрабатываемой детали из другого металла, который растворен подходящим средством. Из данной статьи вы узнаете, как покрыть медью металл в домашних условиях, чтобы реализовать все последующие свои задумки с заготовкой.
Для чего это нужно?
Технология гальваностегии включает в себя создание раствора и образование различных электродов. Во время этого процесса медные ионы, которые растворены в электролите, притягиваются минусовым полюсом обрабатываемой детали на свою поверхностную точку.
Во время этого процесса медные ионы, которые растворены в электролите, притягиваются минусовым полюсом обрабатываемой детали на свою поверхностную точку.
Гальваностегия металлических деталей в промышленности применяется не только как завершающий обрабатывающий процесс. Она может применяться для того, чтобы подготовить детали к последующей операции (к примеру, хромированию, никелированию, серебрению каких-либо предметов).
В домашних условиях чаще всего проводится химическое меднение деталей. Также стоит заметить, что есть множество способов проведения такой процедуры, каждый из которых имеет свои преимущества и недостатки.
Сферы использования гальваностегии
Покрывать медью металл в домашних условиях в последнее время стало очень полезно. Чаще всего к такой процедуре подходят в следующих целях:
- В декоративных. Например, таким способом состаривают различные детали для того, чтобы придать винтажный вид.
- В гальванопластике. Очень часто наносят медный слой на сувениры, ювелирные украшения.

- В отрасли техники. Это связано с низкой стоимостью омеднения.
- Для нанесения защитно-декоративной прослойки того или иного изделия.
- Для того чтобы реставрировать или восстанавливать какие-либо детали.
Гальваностегия электролитным раствором
Таким способом можно покрыть медью сталь в домашних условиях, а также другие детали за исключением алюминия и цинка.
Для дальнейшей процедуры необходимо подготовить следующие материалы:
- Небольшие пластины из меди.
- Токопроводящая проволока (лучше запастись несколькими метрами).
- Источник тока, напряжение которого не должно быть более, чем 6 В.
- Реостат, чтобы регулировать ток.
- Амперметр.
- Электролит.
Важно! Последний компонент можно приобрести в специальном магазине, а можно и изготовить самостоятельно. Для этого нужно сделать раствор серной кислоты и дистиллированной воды при соотношении 2/100 мл. Нужный раствор получится, когда вы добавите к составу не больше 20 г медного купороса.

Суть работы заключается в следующем:
- Очистить обрабатываемую деталь наждачной бумагой — это нужно для того, чтобы снять оксидную пленку. Далее покрыть медью металл в домашних условиях будет не так трудно.
- Обезжирить металлическим предмет горячим раствором соды, промыть его чистой водой.
- В подходящую по объему емкость из стекла налить приготовленный электролит.
- Опустить в жидкость две пластины из меди на подготовленных токопроводящих проводках. Между двумя пластинками из меди подвешивается уже обезжиренная деталь на таком же проводке.
Важно! Проследите за тем, чтобы пластины из меди были полность погружены в электролит.
- Далее концы проводов от пластин из меди присоединяются к положительной клемме источника тока, а деталь — к отрицательной. Далее в созданную электросеть нужно подключить амперметр с реостатом. После того, как ток подключится к цепи, реостатом нужно установить его примерно 15 мА на 1 см площади детальной поверхности.

- Далее деталь выдерживается примерно 15-20 минут.
- По истечении времени нужно отключить электропитание и вытащить обрабатываемый металл из раствора.
В конечном итоге вы заметите, что смогли покрыть медью металл в домашних условиях, ведь он полностью покроется тонкой блестящей пленкой.
Важно! Толщина медного слоя будет зависеть от того, как долго была выдержана деталь в электролите.
Гальваностегия другим способом
Данный способ отлично подойдет для металлов-исключений, что были названы ранее — цинка и алюминия.
Алгоритм работы:
- Вооружиться многожильным проводом из меди, снять изоляцию с обоих его концов.
- Растеребить мягкий провод с одной стороны, получив имитированную кисточку. Привязать к этому концу предмет, похожий на рукоятку.
- Противоположную сторону провода необходимо соединить к плюсовой клемме источника электротока.
Важно! Напряжение должно быть не более, чем 6 В.

- Подготовить электролит описанным выше способом, вылить его в широкую тару — это нужно для удобства макания туда “кисточки”.
- Положить внутрь подготовленной емкости небольшую деталь из металла. Соединить ее, используя при этом провод, к отрицательной клемме токового источника также с напряжением 6 В.
Важно! Деталь должна быть предварительно очищена и обезжирена.
- Процесс покрытия алюминия медью в домашних условиях заключается в следующем: кистообразный конец провода нужно промакивать электролитным раствором и проводить им по поверхности обрабатываемого металлического предмета, не касаясь его. Дальше — отрицательно заряженный металл притянет к себе медные ионы и ее поверхность приобретет медную пленку.
Важно! Следите за тем, чтобы между концом растеребленной проволоки и металла был маленький слой электролитного раствора (и катод, и анод обязательно должны быть смочены этим раствором).

Когда речь идет о гальванотехнике, сразу же на ум приходят такие технологические операции, как хромирование и цинкование металлоизделий. Но если задать вопрос, а что представляет собой гальваностегия, то ответит не каждый – проверено. Хотя ничего сверхнового данный термин не подразумевает.
Проще говоря, это методика покрытия тончайшим слоем металла любого материала, будь-то сталь, алюминий, древесина или пластик. С тем, как произвести меднение какого-либо образца в домашних условиях, мы и разберемся.
Общая информация
Меднение – методика отчасти более универсальная, чем то же цинкование. Для каких целей оно проводится?
- Защита образцов от цементации перед их раскроем способом резания, а также от коррозии.
- Устранение дефектов на поверхностях деталей, когда иные способы неприемлемы или трудны в реализации. К примеру, если основа характеризуется сложным рельефом.
- Декорирование изделий.
- Создание копий образцов из других материалов.

- Подготовка деталей из стали к , серебрению, золочению. В подобных случаях меднение является лишь одним из этапов работы по поверхностной обработке материала.
- Для создания сегментов «под пайку».
Вряд ли читателя заинтересуют такие нюансы, как классификация меди (рафинированная, бескислородная, общего применения), различные варианты растворов, использующихся при меднении, характеристики материалов и подобные вещи. Далее рассмотрены лишь простейшие методы нанесения Cu на любую поверхность, которые несложно организовать в домашних условиях, без каких-либо сложностей и финансовых затрат.
Меднение в электролите
Такая методика подходит лишь для покрытия слоем Cu металлических деталей. По сути, технология мало чем отличается от того же цинкования в домашних условиях.
Подготовка
Оборудование понадобится простейшее:
Ванночка (емкость) стеклянная.
Ее вместительность определяется габаритами обрабатываемой детали.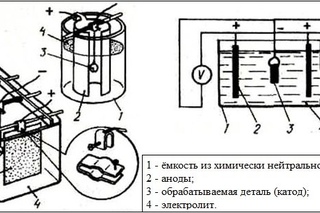 Даже литровая банка или стакан – как варианты.
Даже литровая банка или стакан – как варианты.
Медные электроды. Как правило, используются два. Это позволяет более качественно покрыть заготовку слоем со всех сторон и упрощает сам процесс. По ходу работы не придется периодически менять положение детали относительно электрода. Что именно использовать, зависит от конкретной ситуации – пластины из меди, куски толстой проволоки. Это непринципиально.
Источник тока и соединительные провода. Достаточно даже маломощного блока питания, на 6 – 8 В. Если в БП нет встроенного амперметра и не предусмотрена плавная регулировка напряжения, то придется использовать соответствующий прибор и реостат как отдельные элементы электрической цепи. Примерная схема, которую собирают для меднения деталей, показана на рисунке.
Электролит. Можно использовать покупной раствор, хотя придется и поискать. Если же его готовить самому, то на 100 мл воды дистиллированной понадобится серная кислота (3 мл) и медный купорос (20 г) – не дефицит.
Процесс меднения
- Деталь зачищается от наслоений. При необходимости – протравливается, погружается в специальные растворы для удаления инородных фракций. Что именно использовать, зависит от степени и вида загрязнения.
- Обезжиривание образца. Самый простой способ – окунуть в раствор соды (горячий), а потом промыть водой для удаления ее остатков.
- В емкость наливается приготовленный состав и помещаются электроды. Уровень раствора выбирается так, чтобы он полностью покрывал обрабатываемую деталь.
- Погружение изделия. Оно подвязывается на проводе, который соединяется с «–» БП. Необходимо проследить, чтобы заготовка не касалась стенок ванночки, ее дна и электродов.
После включения напряжения величина тока постепенно повышается до расчетного значения, и в таком режиме обработка осуществляется в течение ⅓ часа (время ориентировочное). Если меднение проводится впервые, то следует контролировать данный процесс. О том, что деталь можно вынимать из емкости, судят по оттенку ее поверхности и равномерности покрытия (отсутствию необработанных участков, раковин, вкраплений и так далее).
Остается лишь смыть с образца остатки электролита и просушить. Получается, что эта технология для реализации в домашних условиях никакой сложности не представляет.
Меднение без ванночки
Данным способом можно наносить металлическое покрытие на любые материалы. Суть заключается в «обмазке» (без прямого контакта) заготовки электролитом специальной кисточкой, щетинки которой – медные проволочки. Недостаток этой технологии в том, что добиться качественного меднения рельефных поверхностей вряд ли удастся. По крайней мере, понадобится много времени и усилий, чтобы тщательно обработать все «щели» и «выбоины».
Особенности подготовительного этапа
Кисточка. В домашних условиях ее делают из многожильного медного проводника. Снять изоляцию и «распушить» один его конец – не проблема. Чтобы было удобнее работать, стоит подумать, из чего изготовить рукоятку кисточки. Ею придется водить по поверхности образца, а с учетом того, что провода гибкие, такое меднение станет испытанием для мастера. Как вариант – подвязать «рабочую часть» к карандашу, пластиковому корпусу шариковой ручки. Догадаться несложно.
Тара. Деталь перед меднением укладывается на любую подходящую посуду. Для удобства работы она не должна иметь высоких бортиков. Оптимальный вариант – тарелка. Плюс к этому – емкость, в которой будет электролит. В нее придется постоянно опускать кисточку, поэтому и здесь выбор не затруднен. Подойдет и стакан, если образец небольшой и раствора понадобится немного. Соответственно, вся тара предварительно обрабатывается – моется, чистится, кипятится, обезжиривается.
Сборка схемы. Аналогично предыдущему способу. Кисточка выполняет функцию анода, поэтому ее к «+» БП, а покрываемая деталь является катодом (к «–»).
Процесс меднения
Для обеспечения неразрывности электрической цепи в посуду наливается электролит, так, чтобы его уровень превышал высоту детали. Кисточкой, которая периодически также обмакивается в растворе (для этого он и заливается в отдельную тару), необходимо водить по-над образцом. В результате его поверхность покрывается слоем меди. По сути, производится ее напыление.
Понятно, что такой процесс в исполнении более сложный, так как проводится в «ручном» режиме. Необходимо постоянно следить, чтобы между кистью и обрабатываемой основой был небольшой зазор. Но и это не главное. Его неизменность – одно из условий равномерности покрытия.
В каких случаях целесообразно использовать такой способ меднения
- Если материал образца не является токопроводящим.
- При больших габаритах детали. Подобрать в домашних условиях ванночку соответствующих размеров, к примеру, для люстры, вряд ли получится.
Как определить требуемые параметры блока питания? Для плотности тока при меднении нормой считаются 0,5 А/дм² образца, который предстоит покрыть защитным слоем.
- Превышение расчетного значения чревато тем, что медь сильно потемнеет, к тому же не будет прочно держаться на основе.
- При сложной конфигурации детали, наличии множества выступов, заостренных сегментов плотность тока берется меньшей, примерно в 2,5 раза.
Медь довольно быстро окисляется. Перед началом процесса обработки изделия электроды следует хорошо зачистить.
Время выдержки детали в растворе выбирается исходя из того, какой толщины слой необходимо получить при меднении. Зависимость прямая – чем дольше идет обработка, тем толще покрытие.
При необходимости восстановления внешнего вида истершихся элементов фурнитуры (мебельной или иной) их меднение – неплохой выход из положения.
Автор не единожды сталкивался с тем, что люди, озабоченные проблемами экологии, сразу же задаются вопросом – а как в домашних условиях организовать утилизацию отработки? Ведь электролит не вечен, и использовать его всю жизнь точно не получится. Кстати, вполне резонное и более чем справедливое замечание.
Есть неплохое решение – собирать оставшуюся после меднения «бурду» в отдельной стеклянной емкости. Зачем? Пригодится. Этот раствор отлично подходит для обработки древесины. Ваш покорный слуга, читатель, сам пропитывал им лаги перед настилом полов на даче. Учитывая, что зимой она не отапливается, условия эксплуатации материала понятны. Когда спустя 12 лет потребовалось переложить половицы, выяснилось, что лаги – как новенькие. Не было даже малейшего намека на какую-то плесень, следы гнили.
Так как любому из нас приходится заниматься если не строительством, то уж ремонтом обязательно, нет смысла куда-то потихонечку, подальше от сторонних глаз, сливать использованный электролит. Не по-хозяйски это.
Меднение – это технологический процесс, позволяющий наносить на металл, а также другие материалы слой меди толщиной от 1 до 300 мкм. Покрытие медным слоем обеспечивает хорошую адгезию покрытий и при увеличении толщины покрытий придает блеск изделиям, устраняет небольшие дефекты, позволяет создавать копии вещи. Удивительно, но все это можно делать и самим. Сегодня мы расскажем, как осуществить меднение в домашних условиях.
Гальваника медью в домашних условиях: общие сведения
С технической точки зрения обработка – это электрохимический процесс. В процессе всегда есть два «участника» анод+электролит (источник металла) и деталь.
Технология процесса достаточно проста. Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Среди основных этапов:
- Подготовка поверхности (механическая и химическая).
- Нанесение подслойного покрытия (если необходимо)
- Меднение в соответствующем исходному металлу электролите.
Для декоративного гальванического меднения подойдут электролиты матового и блестящего меднения. После нанесения слоя, можно обработать поверхность в электролитах серебра, золота никеля и т.д.
Необходимые инструменты
«Ингредиенты», без которых процесс не состоится, реально подготовить самим. Наши специалисты
утверждают, что прежде всего, нужны:
- Источник постоянного тока.Выбирается в зависимости от размера изделия.
- Аноды. Анодные пластины выполняют несколько функций. В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
- Рабочий электролит. Кислотный, щелочной или пирофосфорный раствор. Состав электролита выбирается в зависимости от исходного металла. Необходимо помнить, что любой электролит не универсален и подойдет не для всех работ.
Подготовка материала
Как правильно подготовить простой электролит меднения.
Стоит отметить, что химические реактивы для меднения найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
- Дистиллированная вода (или бидистиллят).
- Медный купорос.
- Соляная или другая кислота.
Готовый раствор имеет яркий синий цвет, запаха нет. Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах. Обязательно следует указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.
Подготовка материала
Химическое меднение является альтернативой электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды материалов подвергаются очистке по-разному:
- Сталь . Обезжиривать сталь можно раствором из едкого натрия и едкого калия при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
- Медь и сплавы. Обезжиривание осуществляется едким натрием, нагретым предварительно до 40°, около 10 минут.
- Чугун. Для процесса обезжиривания нужен раствор из едкого натра, жидкого стекла, карбоната натрия и фосфата натрия при нагревании до 90°.
- Вольфрам. Меднение вольфрама в домашних условиях начинается с чистки предмета от грязи и прочих дефектов наждачной бумагой.
Техника безопасности
Несмотря на возможность гальваники в домашних условиях, процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому следует неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью дома – работайте только в нежилом, хорошо проветриваемом помещении. Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты нужно:
- Постоянно быть в респираторе, чтобы обезопасить дыхательные пути. лучше всего использовать вытяжку.
- Защитить руки прочными прорезиненными перчатками.
- Надеть специальную форму или клеенчатый фартук, противоожоговую обувь.
- Не забыть очки для безопасности зрительных органов.
- Не приносить в помещение еду и питье.
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Гальваника в домашних условиях: меднение
Почему в гальванике столь востребована именно медь? Она имеет высокую адгезию (иными словами – сцепление) к самым разным материалам. Это значит, что она превосходно держится на стальных и прочих изделиях, не отлетая и не скалываясь.
Медь – красивый яркий металл, внешне напоминает самородки розово-красного оттенка. Материал проводит не только тепло, но и электрический ток – отсюда и высокий спрос в сфере электротехники и приборостроении. Однако чистую медь найти сложно. Чаще она поставляется с различными примесями.
Медные покрытия:
- Отличаются малым сопротивлением, что используется в электротехнике
- Скрывает мелкие недочеты поверхности.
- Быстро окисляется, что используют для получения эффекта «антик».
Технологий нанесения покрытия существует две. Одна происходит путем погружения изделия в раствор электролиты (с подачей тока или без). Второй же способ – это метод селективного нанесения покрытия без погружения в раствор. Рассмотрим оба.
Метод погружения
Поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
- Анодную пластину (можно две) помещают в емкость, которую будем называть ванной. На аноды замыкают положительную клемму.
- Между анодами на любом удобном проводнике подвешивается деталь, к ней подводят отрицательный полюс от блока питания.
- Готовый раствор вливается в ванночку – при этом уровень покрытия должен быть выше, чем расположена деталь.
- После подключения электродов к источнику тока выставляют рабочий ток. Это примерно 1 А/кв.дм. покрытия.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Покрытие без погружения
Данный способ имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшие толщины покрытий. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Порядок действий:
- Готовят «тампон» для нанесения покрытия. Берут медный проводник и наматывают кусок искусственной ткани (полиэстер подойдет).
- Противоположный конец проводника подсоединяют к положительной клемме источника напряжения.
- Электролитным раствором наполняют емкость – так удобнее окунать карандаш.
- Деталь аккуратно очищают и обезжиривают, а потом помещают в пустую ванночку. Там изделие подсоединяется к отрицательной клемме.
- Тампон смачивают в растворе. Затем им проводят по поверхности изделия, закрашивая ее постепенно.
Процесс длится до момента покрытия медным слоем изделия.
Особенности гальванопластики
Гальванопластика — это процесс нанесения меди на проводящую или непроводящую поверхность изделия с последующим снятием покрытия с негативной матрицы. Таким образом можно получить множество очень точных копий с одного изделия. При этом требуется наращивание меди толщиной не менее 200 мкм, чтобы изделие получилось прочным.
Важно учесть, что, если поверхность изделия не имеет свойств проводника, то потребуется больше усилий – а именно, особое предварительное покрытие графитом, серебром или медью. Основным материалом для осуществления гальванопластики традиционно считается медь, но можно выращивать матрицы из серебра чистотой 9999.
Обучение гальванике
Можно сделать вывод, что меднение сегодня — это один из наиболее актуальных гальванотехнических процессов, обучиться которому может каждый. Компания «6 микрон» проводит обучение по направлению «Гальваника» для всех желающих! Вы сможете выбрать удобную для Вас программу обучения, которая лучше всего подойдет под Вашу техническую задачу. Все интересующие вопросы можно задать по телефону или по электронной почте, наши технологи помогут Вам определиться с подходящим курсом для обучения.
Видео руководство по меднению деталей в домашних условиях:технологический процесс и необходимое оборудование
Что такое гальваника и с чем ее едят?
Гальваникой называют раздел электрохимии, включающий в себя два подраздела, которые изучают осаждение электролитов на поверхности металла с разными целями. Например, защита от коррозии. В жизни такое же название носит и сам процесс покрытия изделий, например, хромом или медью. В последнее время стала очень популярна декоративная гальваника в домашних условиях, которая приносит немалый доход тем, кто готов поработать.
Что в составе
Гальваника — достаточно размытое определение, включающее в себя несколько процессов, название которых связано с применением различных электролитов. Пример — золочение, т. е. покрытие тонким слоем золота, или хромирование. Также популярно медение и серебрение.
Гальваника в домашних условиях. Возможно ли это?
Декоративное покрытие различных предметов металлом становится все популярнее среди начинающих предпринимателей. Прежде всего благодаря тому, что стартовые вложения сведены к минимуму. Но гальваника в домашних условиях — не самая лучшая идея по одной простой причине: токсично. Лучше подобрать хорошо проветриваемое нежилое помещение. И прочитать соответствующую литературу на эту тему, чтобы быть готовым ко всему.
Необходимое оборудование для гальваники
Все необходимое для первого опыта возможно сделать своими руками или приобрести без особых затруднений. Сам процесс связан с действием силы тока, поэтому необходим блок питания. У него должен быть регулятор напряжения, а сила тока на выходе — один Ампер. Также нужна небольшая ванночка из токонепроводящего, химически стойкого материала, например пластиковый лоток с тонкими стенками. Также домашняя гальваника требует наличия специальной кисточки или ручки, которая представляет собой полую форму, в которую заливается электролит.
Технологический процесс
Гальванические процессы происходят под действием тока. В специальную ванночку устанавливаются два анода и заливается электролит. Обрабатываемую деталь подключаем к «минусу», а аноды — к «плюсу». При замыкании цепи металл, содержащийся в электролите, осаждается на рабочий объект. Приготовление раствора для каждого металла индивидуально, причем пропорции необходимо строго соблюдать, так же как и силу тока, изменение которой может значительно повлиять на процесс.
Гальваника в домашних условиях. Подготовка деталей
Прежде чем приступать к самому процессу, с рабочих объектов необходимо удалить загрязнения. В некоторых случаях достаточно обойтись лишь обезжириванием поверхности, но иногда приходится прибегать к шлифовке и другим более сложным способам.
Домашняя гальваника опасна для здоровья
Химический процесс всегда связан с риском, поэтому необходимо соблюдать элементарные правила безопасности:
- позаботьтесь о наличии заземления;
- хорошая вентиляция помещения обязательна;
- необходимо соблюдать правила личной безопасности при работе с вредными веществами.
В качестве заключения
Помните, что гальваника — очень опасный процесс, связанный с применением активных веществ, которые могут нанести вред вашему здоровью и имуществу. Поэтому внимательно изучите все опасные аспекты и лишь тогда принимайтесь за работу.
Метод цинкования – один из самых распространенных для создания надежной защиты для металла от коррозии. Он отличается простотой и дешевизной. Поэтому такой способ обработки можно выполнять в домашних условиях, для чего необходимо лишь соблюдать определенные условия.
Цинкование как распространенный способ коррозийной защиты металлов
При создании качественных и долговечных металлических покрытий чаще всего применяют именно технологию цинкования. Это объясняется невысокой стоимостью расходных материалов и отличным результатом. Само цинкование происходит по простейшей технологии. Для ее осуществления не нужны дополнительные расходы и много усилий, что позволяет проводить подобную обработку в домашних условиях.
Цинковое покрытие формируется в результате того, что цинк вступает в реакцию окисления с кислородом, находящимся в составе воздуха. В последующем на поверхности обрабатываемого металла образуется прочная защитная пленка, которая ограждает его от негативного воздействия внешней среды.
Цинк является более активным металлом, чем железо или сталь. Поэтому он в первую очередь взаимодействует с кислородом и водой, предотвращая коррозию. Даже если на поверхности изделий из металла присутствует хоть часть покрытия, оно защищает его от разрушения.
Проведение цинкования в домашних условиях
Технологический процесс цинкования подразумевает под собой осаждение катионов металла на аноде. Подобная химическая реакция протекает в ванне с электролитом при воздействии электрического тока.
Где найти электролит
В качестве электролита можно использовать любой раствор солей цинка. Самыми популярными и легкодоступными считаются хлорид цинка и соляная кислота. Также электролит с необходимыми свойствами можно получить методом травления цинка в серной кислоте. Эту реакцию следует проводить очень осторожно. Она сопровождается выделением большого количества тепловой энергии и взрывоопасного водорода.
Травление цинка в серной кислоте с выделением водорода и получением солей цинка
Как получить цинк
Для цинкования в домашних условиях необходимо подготовить цинк, который можно получить следующими способами:
- используя обычные солевые батарейки;
- плавкие предохранители времен Советского Союза;
- любые детали с цинковым покрытием;
- чистый металл, который можно найти в соответствующих магазинах, где продаются химические реактивы.
Подготовка к выполнению процедуры
Для создания качественного металлического покрытия следует выполнить несколько подготовительных операций:
- подготавливают гальваническую ванну. Ее роль может выполнять любая стеклянная или пластиковая тара;
- устанавливают штативы для анода и катода;
- электролит не должен содержать в составе нерастворенные кристаллы соли , для чего дополнительно вводят дистиллированную воду;
- роль анода выполняет цинковая пластина. Чем больше ее площадь, тем качественнее получится покрытие;
- к аноду присоединяется плюс от источника питания. Данных элементов при желании может быть несколько;
- к катоду присоединяется минус. На его поверхности будут осаждаться частицы цинка;
- катод должен быть очищен от ржавчины и любых загрязнений. Перед обработкой его дополнительно окунают в раствор кислоты;
- катод должен находиться на одном расстоянии от анода, чтобы получилось равномерное покрытие со всех сторон;
- в качестве источника питания применяют любой аккумулятор или блок питания с постоянным током на выходе;
- чем больше сила тока и вольтаж, тем быстрее будет происходить реакция и тем рыхлее получится защитная пленка;
- при использовании автомобильного аккумулятора в цепь включают лампочку накаливания до 20 Вт для снижения силы тока.
Устройство для цинкования в домашних условиях
Технология создания цинковой пленки
Для создания качественного защитного покрытия на поверхности металла после проведенных подготовительных операций источник тока подключают к сети, а катод окунают в гальваническую ванну. Данный процесс должен проходить без бурного кипения. Если такое наблюдается, можно заподозрить слишком большую силу тока в системе. Чтобы снизить ее, в электрическую цепь присоединяют несколько дополнительных потребителей.
Постепенно на поверхности катода будет формироваться металлическое покрытие. Чем дольше протекает этот процесс, тем больше будет толщина защитного слоя на металле.
Популярные методы
Существует много эффективных химических способов выполнения цинкования, каждый из которых имеет свои преимущества и недостатки. В любом случае созданное покрытие будет служить долго, если не подвергать его механическим воздействиям и правильно выбрать толщину защитного слоя с учетом особенностей эксплуатации изделий.
Горячий метод
Данный способ цинкования является одним из самых эффективных. После проведения подобной обработки удается создать надежное покрытие, которое надолго остается на поверхности металлических изделий. Недостатком горячего метода является его вредность для окружающей среды.
Для выполнения данной обработки необходимо придерживаться следующей технологии:
- подготовка. Поверхность металла обезжиривают, проводят травление;
- после выполнения подготовительных процедур деталь промывают и высушивают;
- изделий из металла опускают в емкость с цинковым раствором.
Такой метод цинкования не подходит для обработки больших по площади деталей и требует определенной подготовки, поиска подходящих емкостей.
Холодный метод
Данный метод обработки подразумевает окраску металлоизделий специальными смесями. Они содержат в составе цинк, что позволяет в кратчайшие сроки сформировать на поверхности надежное покрытие. Наносят такую краску обычным способом – валиком, кистью, краскопультом. Такой метод обработки идеален для деталей, которые невозможно покрыть защитным слоем обычным горячим цинкованием.
Гальваническое цинкование
Схема гальванического цинкования
Такое цинкование в домашних условиях проводится с применением электрохимических воздействий на металл. При его выполнении на поверхности металла образуется тонкая защитная пленка, которая эффективно защищает металл от внешнего негативного воздействия.
Для обработки изделие помещают в специальную емкость, где находится цинковая пластина. После этого подводится электричество. Именно оно переносит частицы цинка с пластин на поверхность обрабатываемых изделий.
Основным недостатком данного метода называют его дороговизну. Также в процессе обработки металла остаются опасные яды, которые требуют специальной утилизации.
Термодиффузионное цинкование
При выполнении термодиффузионного цинкования создается среда, которая характеризуется наличием высоких температурных показателей. Примерно при +2600°С цинк расщепляется на мелкие частицы, которые оседают на поверхности металлических изделий. Основным преимуществом данного метода цинкования является то, что в результате его выполнения образуется особенно толстый защитный слой.
Процесс нанесения защитного покрытия на изделия из металла осуществляется в специальной камере закрытого типа. Вначале на поверхность детали наносится порошковый цинк, после чего она подвергается нагреву. Данная технология применяется исключительно в промышленных условиях. Дома ее использовать очень сложно, дорого и небезопасно.
Преимуществом термодиффузионного цинкования называют его безопасность для окружающей среды. Создаваемое покрытие имеет значительную толщину, что обеспечивает отличные защитные качества.
Нанесение цинка осуществляется при помощи интенсивного газового потока. После выполнения подобной обработки поверхность обязательно окрашивают. Несмотря на особенности подобной технологии, она обеспечивает высокое качество и долгий срок службы обрабатываемых деталей.
Те, кто хорошо помнит школьную программу по курсу «Химия», сразу ответят на вопрос, что такое гальваника. Тем, кто немного подзабыл, напомним, что это раздел электрохимии, так называют процесс, когда на практически любое изделие наносится покрытие из металла. Этот процесс применяется и в промышленных масштабах, например, как при оцинковке или хромировании металлических изделий, так и при изготовлении декоративных предметов.
Процесс оседания электролитов на нужную поверхность достаточно сложный, требует соблюдения техники безопасности и определенных навыков обработки дома. Гальваника в домашних условиях не позволит вам усилить прочность металлического изделия (для этого нужны промышленные мощности), но может использоваться для декорирования отдельных предметов.
Для организации процесса вам потребуется:
- Гальваническая ванна своими руками – банка (из стекла или прочной пластмассы, достаточна большая, чтобы поместилось обрабатываемое изделие, термостойкая) с раствором электролита.
- Провод, разделенный на анод («плюс») и катод («минус»). При этом аноды должны быть по площади больше, чем обрабатываемое изделие. Они проводят ток в электролит и замещают убыль металла в нем, того, что будет оседать на гальванируемом изделии.
- Оборудование для взвешивания, например, точные электронные весы.
- Источник постоянного тока с регулировкой напряжения, домашняя розетка не подойдет.
- Электроплитка с обязательной регулировкой температурного режима.
Сам процесс нанесения гальванического покрытия в домашних условиях достаточно прост: в емкости развести электролит, нагреть, погрузить туда аноды, подключенные к «плюсу», на расстоянии закрепить гальванируемое изделие (в нашем случае – катод), который подключают к «минусу». При подключении к источнику тока металл из электролита начинает оседать на «минусе», то есть на изделии.
Что нужно для приготовления электролита?
Как сделать электролит дома? Сначала выберем правильную посуду для хранения: это должна быть емкость из неактивного вещества (стекла или пластика), прочная, плотно закрывающаяся крышкой, чтобы избежать доступ кислорода для электролита.
Совет! Выпрямитель для гальваники своими руками легко получается из обычного автомобильного аккумулятора.
Химия – наука точная. Каждое используемое вещество придется отмерять с точностью до сотых грамма. Вам потребуется качественное весовое оборудование, удобнее всего электронное. Если возможности или желания купить весы нет – берите мелочь советского периода, монеты тогда имели точный вес.
Самое труднодоступное для простого гражданина – приобретение реактивов для изготовления электролита. Многие вещества запрещены к продаже физическим лицам, только промышленным предприятиям при наличии особого разрешения. Простым людям опасные реактивы не продадут!
На видео: Ток 60А в домашних условиях или кустарная гальваника.
Как подготовить изделие
Собрав вес необходимых компонентов, подготовив емкости, систему подогрева и источник тока, переходим к подготовке изделия, которое хотим обработать.
Чтобы металл из электролита ровным слоем осел на предмет, его нужно очень хорошо очистить, иначе гальваническое покрытие в домашних условиях получится неровным и непрочным. Некоторые предметы достаточно будет просто обезжирить, некоторые потребуют чистки наждачной бумагой и шлифовки, чтобы удалить с поверхности коррозию и «заусенцы».
Важно! Качественное обезжиривание обеспечивает раствор ацетона, спирт и даже бензин.
Стальные изделия держат несколько минут в растворе фосфорнокислого натрия, разогретого до 90 градусов. Цветные металлы обезжиривают тоже в растворе натрия, только без подогрева.
Техника безопасности
Прежде чем начинать процесс гальванизации, не забудьте о технике безопасности. Гальваника своими руками не подразумевает проведения манипуляций, например, на кухне. Речь идет скорее о гараже или сарае, нежилом месте с хорошей вентиляцией, где можно организовать заземление.
Важно! Не отравитесь ядовитыми испарениями! Гальванизация может нанести реальный вред здоровью. Организуйте вытяжку и закройте лицо маской-респиратором.
На руки обязательны плотные резиновые перчатки. Глаза защитите очками. Перед началом манипуляций почитайте специальную литературу. При каких-либо проявлениях недомогания незамедлительно обратитесь к врачу.
Варианты обработки
Нанесение покрытия из никеля на металлические предметы – несложный процесс, в результате которого ваши изделия получат роскошный блестящий вид, станут более стойкими к дождю и прочим явлениям.
От вас потребуется:
- Приготовить электролит для гальваники, смешав сульфат никеля, натрий, магний, хлористый натрий (поваренная соль) и борную кислоту. Проверьте рН, он должен быть в диапазоне 4–5.
- Разогрейте электролит до 25 градусов.
- Поместите в емкость изделие и подключите ток 1,2 А/кв. дм.
- Примерное время – около получаса.
Указанное время зависит от таких факторов, как размер изделия, плотность тока и температура электролита. Чем больше время, тем толще получится слой наносимого никеля. По окончании промойте предмет и отполируйте любой полировочной мазью.
На видео: химическое никелирование.
Хромирование
Один из самых популярных способов придания прочности и внешнего вида изделиям из металла – хромирование. Пусть дома добиться высокой прочности не удастся, для этого нужен ток плотностью 100 А/кв. дм., декоративное покрытие нанести вы все же сможете.
Покрытие из хрома пористое. Перед его применением предмет покрывают медью или никелем. Зато домашнее хромирование позволяет добиться большего разнообразия оттенков, что достигается разной температурой электролита: чем она выше, тем более блестящим получится покрытие.
Процесс хромирования в домашних условиях выглядит следующим образом:
- Аноды из свинца, олова и сурьмы (85%/11%/4%).
- Погрузите изделие в электролит нужной вам температуры и подождите около получаса.
- Промойте в слабом растворе пищевой соды, просушите, отполируйте.
На видео: декоративное хромирование в домашних условиях.
Меднение
Покрытие поверхностей металлов медью в домашних условиях применяют для создания слоя, который будет впоследствии проводить ток, или для защиты от коррозии.
Сделать гальванику медью дома на черных металлах в домашних условиях невозможно, поскольку для этого используются смертельно опасные цианиды. Первоначально стальные и чугунные предметы надо никелировать, а затем уже проводить гальванизацию меднением с использованием солей медного купороса, разведенных в серной кислоте. Покрытие медью алюминиевых изделий потребует первоначальной очистки последних от окиси в электролите, содержащем серную кислоту, а потом гальванизируют также, как и сталь.
На видео: гальваническое меднение.
Цинкование
Самый простой в домашнем исполнении метод гальванизации – это обработка цинком. Его используют для защиты предметов из металла (электропроводящих и неэлектропроводящих) от появления коррозии. При цинковании в электролит в качестве анода погружают пластинку из цинка, соответствующую по площади оцинковываемому предмету, и подключают к источнику тока.
В состав электролита входит: сернокислый цинк (200 г), сернокислый аммоний (50 г), уксусный натрий (15 г) из расчета на 1 л воды. Примерно за полчаса анод растворится и его молекулы плотным слоем покроют обрабатываемый предмет.
На видео: оцинковка металла в домашних условиях.
Латунирование
Самый декоративный метод гальваники – латунирование (нанесение пленки из сплава меди и цинка). Покрытые латунью изделия используют для мебельной фурнитуры, в качестве дверных ручек и т.д. Латунь придает предметам благородный золотой цвет и насыщенный блеск.
Электролит для латунирования должен содержать соли меди и цинка, растворенные в растворе цианида. Данный вид гальванизации также не рекомендуется для применения в домашних условиях из-за возможности отравления цианидами.
Каким бы ни был увлекательным процесс гальванизации, повторять его дома без предварительной подготовки не рекомендуется – может быть опасно для жизни. Оборудование стоит денег, а некоторые необходимые для изготовления электролитов реагенты вы просто не сможете приобрести. Затевать процесс, например, для хромирования одной детали того не стоит – дешевле будет обратиться в специализированные предприятия.
Серебрение и золочение
Гальваническое нанесение серебра на изделия имеет не только декоративное предназначение, оно также защищает от появления коррозии и образует электропроводящее покрытие. Как и в случае с медью, чугунину и сталь предварительно покрывают никелем, затем серебрят.
Электролит для серебрения содержит:
- хлористое серебро;
- железноцианистый калий;
- кальцинированную соду;
- дистиллированную воду.
Электролит необходимо подогреть до температуры до 20 градусов. Высокой мощности не требуется – хватит 0,1 А/кв. дм. Анодом станет пластина из графита, размером, соответствующем размеру гальванизируемого изделия.
Гальваника золотом — наиболее декоративный метод.
Для этого потребуется подогретый раствор золота в пропорциях 5 г на 1 л воды, смешанный с синеродистым калием. Можно использовать и холодный электролит, но тогда золота необходимо будет в 3 раза больше.
Будьте крайне аккуратны – испарения синеродистой кислоты крайне опасны, как в горячем виде, так и в холодном. Не пренебрегайте вентиляцией, не допускайте попадания ее на открытые участки кожи. При возможности замените её на железистосинеродистый калий.
Предварительно тщательно очистите изделие. Если оно выполнено из черного металла, покройте сначала медью, затем золотите. Чтобы золото лучше «приставало», окуните изделие в азотнокислую ртуть.
На видео: гальваническое золочение серебряной ложки.
Главное правило: аккуратно при использовании тока – он должен быть не мощнее 1 А/кв. дм. Более сильный ток приведет к тому, что золото будет черными хлопьями падать на дно емкости, а гальванизируемый предмет вместо золотого превратится в бурый. После окончания процесса изделие просушивают и полируют с применением полировочной мази.
Гальванопластика и гальваностегия
Что такое гальванопластика? Это метод, который применяется для изготовления точных копий изделий, метод копирования. Его применяют, когда необходимо сделать копию с предметов тончайшей конфигурации – пластинок, чипов и схем. Гальваностегия позволяет усилить механические свойства одного металла путем нанесения на него слоя другого металла, например, хромирование и никелирование стали, никелирование меди и т.д.
Гальванопластика и гальваностегия имеют схожую природу, отличаются лишь способом подготовки металла перед обработкой. При осуществлении гальваностегии поверхность металла должна быть максимально подготовленной для сцепления с наносимым металлом. Метод гальванопластики, наоборот, подразумевает свободное отделение наносимого металла.
Для гальванопластических процессов применяют чаще всего медь, никель и серебро, а в гальваностегических – практически все виды металлов. Гальванопластика в домашних условиях проводится на том же оборудовании, что и другие гальванические процессы.
Под гальванопластическую ванну прекрасно подойдет большая стеклянная емкость.Её размеры зависят от величины гальванизируемого предмета, поскольку он не должен располагаться слишком близко от анодной пластины.
Гальванопластика дома может применяться для изготовления копий предметов небольшого размера по предварительно отлитым из легкоплавких металлов формам.
Мастер-класс по гальванике (1 видео)
Предметы с гальваническим покрытием (17 фото)
Гальваника представляет собой раздел электрохимической науки, которая изучает осаждение некоторых элементов на любую поверхность. С помощью гальваники в домашних условиях или в промышленности можно нанести на изделие тонкий слой металла, который будет выступать в роли защитного слоя или выполнять декоративные функции. В последнее время декоративное покрытие набирает популярность у тех, кто хочет сделать оригинальный подарок своим друзьям и родным.
Общие сведения
Покрытие гальваникой бывает технологическим или декоративно-защитным. Это тонкий металлический тонкий слой, который в зависимости от гальванических элементов может выполнять эстетические функции. Гальванопластика не увеличивает прочность изделия, поскольку в этом случае требуются большие производственные мощности, но для красоты и придания «свежести» вполне подойдет.
Гальванические реакции происходят с помощью постоянного электрического тока. В специальную емкость-диэлектрик наливают раствор — электролит, в который погружают два анода. Аноды должны быть изготовлены из металла, который будет осаждаться на покрываемом изделии.
Обрабатываемая деталь присоединяется к минусовому выводу и помещается между анодами. Она выполняет роль катода. Аноды, в свою очередь, присоединяются к плюсовому контакту источника питания. Они становятся частью цепи, проводя ток в электролит и отдавая ему свои металлические элементы. Электролит передает необходимые частицы обрабатываемой детали, они постепенно обволакивают её тонким слоем. Аноды по площади должны превышать в несколько раз размер заготовки.
Другими словами, гальванизация представляет собой перенос молекул металла раствора на изделие в момент протекания через них электротока.
Любой гальванический процесс можно разбить на общие этапы:
- Сборка гальванической установки.
- Подготовка электролитного раствора.
- Обработка и подготовка образца.
- Запуск гальванического процесса.
Оборудование можно подготовить самостоятельно. Сначала подбирается подходящий источник питания. Это может быть батарейка (для обработки изделий небольшого размера) или аккумулятор. Подойдет понижающий блок питания, который выдает на выходе постоянный ток до 12 вольт. Иногда используют инвертор от сварочного аппарата. Подбирается реостат для регулирования силы тока.
Из нейтрального, устойчивого к химически агрессивным веществам материала подбирается широкая и глубокая ванночка. Надо учитывать, что электролитический раствор при гальваническом процессе может нагреваться до девяноста градусов по Цельсию.
Подготавливаются две пластины, которые будут токопроводящими анодами.
Для нагрева ёмкости с электролитом нужен электрический прибор с возможностью плавной регулировки температурного режима. Чаще всего используют подошву утюга или небольшую электроплитку. С их помощью происходит нагрев раствора до необходимой температуры и ускорение реакции.
Химические реактивы необходимо хранить в плотно закупоренной стеклянной посуде. Желательно каждый предмет подписывать.
Потребуются весы для точного измерения массы веществ, поскольку необходимая точность веса компонентов составляет один грамм. Такие весы можно приобрести, а можно сделать самостоятельно, используя вместо гирек старые советские монеты. Вес «желтых» монет точно соответствует их номиналу.
После того как собраны необходимые вещества, найдены ёмкости, собрана электрическая схема с питанием и подготовлена система подогрева, можно заняться чисткой заготовки.
Если недостаточно хорошо почистить деталь, гальваническое покрытие непрочно осядет или будет неравномерным. Иногда хватает простого обезжиривания предмета. Раствор ацетона или спирта может хорошо обезжирить поверхность, можно использовать бензин.
Некоторые мастера держат изделия из стали в разогретом до 90 градусов по Цельсию растворе фосфорнокислого натрия. Цветные металлы можно очищать в том же растворе, не нагревая его.
Если на изделии есть коррозия или другие изъяны, то поверхность заготовки шлифуется наждачной бумагой.
Иногда про технику безопасности при различных работах в домашних условиях рассказывают вскользь. Но при выполнении любых гальванических работ нужно строго соблюдать безопасность.
Опасность заключается в использовании токсичных химических веществ, высокой температуре нагрева раствора и повышенными рисками, которые сопровождают электрохимические реакции.
Лучше всего гальванические работы проводить в гараже или мастерской при обязательном проветривании или вентилировании помещения. Особое внимание следует уделить заземлению оборудования. Нужно соблюдать меры личной безопасности, а именно:
- Дыхательные пути следует защитить респиратором.
- Руки и запястья должны быть спрятаны в высокие и прочные резиновые перчатки.
- Обувь должна защищать от ожогов, а одежда прикрыта клеенчатым фартуком.
- Обязательно ношение специальных защитных очков.
Перед началом работ по меднению в домашних условиях нужно подготовить необходимые материалы и оборудование. Надо позаботится об источнике напряжения и постоянного тока. Существует много рекомендаций касательно силы тока, разброс которого может быть большим. Поэтому желательно иметь реостат с возможностью плавной регулировки напряжения и для постепенного завершения процесса. Источником может служить автомобильный аккумулятор или выпрямитель с напряжением на выходе не больше 12 вольт. Для первых опытов будет достаточно обычной батарейки от 4.5 до 9 вольт.
Затем выбирается ёмкость для электролитического раствора, лучше всего из жаропрочного стекла. В любом случае все ёмкости для электролиза должны быть диэлектриками и выдерживать температуру не менее, чем 80 градусов по Цельсию.
В качестве анодов подойдут два больших медных листа. Они должны перекрывать по размеру заготовку. Из химических реактивов потребуются:
- Купорос медный.
- Кислота соляная либо серная.
- Вода дистиллированная.
Меднение в домашних условиях пользуется заслуженной популярностью, поскольку очень хорошо и надежно держится на стальных изделиях. Главное условие — правильно соблюдать технологию процесса.
Имеется два способа нанесения меди на поверхность:
- Помещение заготовки в раствор электролита.
- Неконтактный способ. В этом случае изделие не погружается в раствор.
Подготавливается и обрабатывается поверхность изделия при помощи тонкого наждака и щеточки. После этого деталь моется в проточной воде, обезжиривается и еще раз промывается.
Этапы процесса омеднения следующие:
- Два медных анода подключают в сеть к положительным контактам и размещают их в стеклянную банку.
- К обработанному изделию подводят контакт с отрицательным значением напряжения и свободно подвешивают между анодами.
- Подключают реостат согласно электрической схеме для возможности регулирования силы тока.
- Подготавливается раствор в правильных пропорциях. На 100 г дистиллированной воды надо 20 г медного купороса и 2−3 г соляной кислоты. Вместо соляной кислоты можно использовать другую.
- Раствор выливается в посуду с медными пластинами и деталью таким образом, чтобы они полностью скрылись под поверхностью раствора.
- Подключается источник напряжения. Реостатом добиваются необходимой силы тока из примерного расчета 10−15 миллиампер на каждый квадратный сантиметр площади детали.
Весь процесс занимает примерно 15−20 минут. После обязательного выключения источника питания и остывания раствора готовое изделие с медным слоем на поверхности вынимается из банки.
Этот метод интересен тем, что его можно использовать для обработки не только стальных предметов, но и сделанных из других материалов. Например, алюминия и цинка. Порядок процесса следующий:
- Из многожильного медного провода изготавливается «кисточка». Конец провода оголяется. Из медных проводков создается подобие кисточки, чтобы затем прикрепить ее к деревянной ручке-держателю.
- Второй конец провода подключается к плюсовому контакту электрической цепи.
- В широкую ёмкость заливается стандартный электролитный раствор из медного купороса и соляной кислоты.
- Предварительно очищенная и промытая металлическая заготовка присоединяется к отрицательному контакту и размещается в пустой ёмкости.
- Импровизированная кисточка окунается в раствор электролита и проводится по поверхности заготовки без контакта. Это действие повторяется до получения результата.
Когда деталь полностью покроется слоем меди, выключается блок питания и процесс завершается. Деталь ополаскивается в воде и просушивается.
Часто с помощью медного электролиза обновляют столовые приборы, сделанные из алюминия. Если нет опыта проведения этого процесса, то можно потренироваться нанести медь на алюминиевые пластинки. Порядок проведения процесса:
Гальванопластика — это электрохимический способ придания предмету определенной формы с помощью осаждения на него металла. Чаще всего этот метод используют при обработке металлом неметаллических предметов или при изготовлении копий ювелирных изделий.
Если при гальванопластике изделие не обладает электропроводящими свойствами, то его предварительно покрывают графитом, иногда бронзой. Затем мастер делает с копии слепок и начинает гальванический процесс. В качестве материала слепка используют гипс, графит или легко плавящийся металл.
Гальваника — это очень интересный и познавательный процесс, но он связан с активными веществами, которые могут навредить здоровью и нанести вред имуществу или окружающей среде. Поэтому перед тем как начинать гальванику своими руками, нужно принять все меры безопасности, изучить немного теории процесса и особенности поведения химических реактивов.
В 1840 году российский учёный-физик немецкого происхождения, Мориц Герман, который после переезда в Российскую империю сменил имя и фамилию на Борис Якоби, пишет работу под длинным названием: «Способ производить, по данным образцам, из медных растворов медные изделия с помощью электричества или Гальванопластика для прикладных искусств». С этого научного труда начинается история гальваники не только в России, но и в мире.
В своих исследованиях Якоби опирался на более ранние работы итальянского физика Луиджи Гальвани, поэтому и назвал процесс гальванопластикой, а емкость в которой происходит сие чудо — гальванической ванной.
В настоящее время гальваника является разделом электрохимии и изучает осаждение электролитов на поверхности металлов. В свою очередь, гальваника разделятся на два больших подотдела:
- Гальванопластика: электрохимический способ копирования. С его помощью наносят достаточно толстый слой металла и как следствие получают точную копию копируемого предмета. В частности, посредством этого метода изготавливают виниловые пластинки и лазерные компакт-диски.
- Гальваностегия: электрохимическая технология покрытия подложки слоем металла, с целью получения более прочного или более декоративного слоя. Часто эти две задачи совмещают.
Посредством процесса гальваностегии можно покрыть слоем металла, захромировать практически любую поверхность: металлическую, пластиковую, деревянную, кожаную. Хромированные сапоги или никелированные ботинки — вещь вполне реальная, но не совсем практичная. Гораздо более востребовано покрытие одного металла другим с целью повышения антикоррозийных, прочностных и эстетических характеристик. Такие процессы, как хромирование, никелирование, меднение, цинкование давно стали обычной практикой крупного промышленного производства.
Химическая металлизация своими руками в домашних условиях. Гальваника в домашних условиях вещь вполне реальная, конечно, при соблюдении определённых требований. Из всех видов домашней гальваники хромировка является, пожалуй, самым сложным видом гальваностегии по двум причинам:
- Техническая сложность процесса.
- Крайняя опасность химических компонентов для здоровья.
Первая техническая сложность
Сложность хромирования состоит в том, что предъявляются очень жёсткие требования к режиму функционирования гальванической ванны. Малейшие отклонения от требуемой плотности тока, температуры и концентрации электролита приводят к резкому изменению качества хромового покрытия, вплоть до брака.
Способность хрома сильно меняться в качественном отношении, в зависимости от температуры электролита и силы тока, активно используется на производстве для получения хромовых покрытий с разной степенью блеска, окрашенности и прочности.
- При температуре электролита от 30−60 градусов поверхность готового изделия будет блестящей.
- Выше 60 градусов — хромовое покрытие будет иметь молочный оттенок.
- Ниже 30 градусов — поверхность матовая.
От концентрации состава электролита хром меняет цвет, а вместе с цветом меняются и прочностные характеристики. Цвет меняется от обычного светлого, до темно-голубого, агатового, синего и, наконец, до практически чёрного. По мере изменения цвета меняется и прочность хромового покрытия. Самый мягкий хром имеет обычный светлый цвет, для его получения требуется комнатная температура и сила тока порядка 5 А/кв.дм. Самое прочное хромовое покрытие соответствует хрому чёрного цвета. Но для получения чёрного хрома необходима сила тока 100 А/кв.дм, что в условиях домашнего производства сделать технически невозможно.
Вторая техническая сложность
Вторая сложность состоит в том, что хром не может непосредственно соединяться со сталью, алюминием, чугуном или железом. Поэтому всегда перед хромированием проводят процесс никелирования. Часто с целью получения более качественного результата проводят несколько последовательных нанесений слоёв: никель, медь, снова никель и только в заключение наносят слой хрома.
При этом нужно иметь в виду, что само по себе хромовое покрытие обладает достаточно противоречивыми характеристиками. С одной стороны, хром обладает высокой механической прочностью (намного выше, чем у никеля), химической инертностью и очень ярким блеском. Но одновременно с этим он очень хрупок и обладает пористой структурой. Поэтому подложка из никеля для слоя хрома является необходимой даже в том случае, если хромирование осуществляется на поверхность металла, с которым у хрома хорошая сцепка, например, медь или латунь.
Таким образом, процесс хромирования в домашних условиях автоматически подразумевает проведение как минимум двух последовательных технологических процессов: никелирования и хромирования.
Опасность для здоровья
Основной компонент электролита для хромирования — оксид хрома (CrO3) или, как его ещё называют, хромовый ангидрид. Так уж получилось, что хромовый ангидрид является сильнейшим ядом и одновременно одним из самых сильных канцерогенов. Смертельная доза для человека при приёме внутрь составляет приблизительно 4−6 грамм, в зависимости от веса индивида. При попадании на открытые участки кожи чистого оксида хрома или его растворов возникают химические ожоги, которые затем переходят в дерматиты и экземы, с последующим перерождением в рак кожи.
При соединении оксида хрома с веществами, имеющими органическую природу, такими как технические растворители, бензин, керосин, происходит мгновенное возгорание и взрыв.
Понятно, что такое «прекрасное» химическое вещество невозможно просто взять и купить в магазине хим. реактивов. Оборот хромового ангидрида жёстко регулируется государством и продажа разрешена только юридическим лицам, имеющим лицензию на соответствующий род деятельности.
Необходимое оборудование
Хромирование на кухне жилой квартиры способен проводить только потенциальный самоубийца. Для того чтобы начать процесс хромирования фары, необходимо иметь для этого специальное помещение, максимально удалённое от жилых построек. Лучше всего для этих целей подойдёт просторная мастерская или гараж. Обязательно наличие хорошей принудительной вентиляции. Предварительно из помещения должны быть удалены все ёмкости с бензином, красками, лаками и прочими растворителями. В обязательном порядке приобретается хороший огнетушитель и прорабатывается вариант запасного выхода из помещения в случае возникновения нештатной ситуации.
Для хромирования необходимо иметь:
- Гальваническая ванна. Либо из стекла, либо из прочного пластика, способного выдерживать повышение температуры до 100 градусов.
- Выпрямитель. Источник постоянного тока с возможностью регулировать выходное напряжение. Параметры — 12В/50А. Если речь идёт о мелких деталях, то можно использовать зарядное устройство для автомобильного аккумулятора.
- Нагреватель. Должен выдерживать долговременное пребывание в агрессивной кислой среде. Например, керамический тэн. Обычный тэн не подойдёт.
- Термометр. С делениями от 0 до 100 градусов. Оптимальная температура для проведения процесса составляет 45−55 градусов.
Нужно иметь в виду, что для оптимизации процесса необходимо оборудовать как минимум две такие установки, одна для хромирования, а вторая для никелирования. В противном случае придётся постоянно менять реактивы в одной ёмкости, что крайне неудобно и затратно.
Три составляющие гальванического процесса
Гальваника в домашних условиях, хромирование — это гальванический процесс. Поэтому для его проведения необходимо наличие трёх составляющих: катода, анода и электролитической среды, в которой будет происходить перенос заряженных частиц металла.
- Катод. Пластина чистого свинца либо сплав свинца с оловом. Необходимо помнить, что площадь катода должна быть больше площади анода. Катод подсоединяется к положительному выходу выпрямителя.
- Анод. Это и есть сама хромируемая деталь. Он должен висеть в среде электролита таким образом, чтобы не касаться стенок и дна емкости. Кроме того, анод ни в коем случае не должен касаться катода.
- Электролит. Для хромирования требуется особо тщательная подготовка электролита.
Приготовление электролита
В набор электролитической жидкости для хромирования входят следующие компоненты:
- Хромовый ангидрид: 250 гр/л.
- Серная кислота: 2−3 гр/л. Химически чистая, концентрированная. Техническая серная кислота не годится.
- Вода дистиллированная.
Вода нагревается до температуры 60−80 градусов. После этого в ней растворяется ангидрид. Раствор чуть охлаждается и затем в него добавляется тонкой струйкой необходимое количество серной кислоты.
Подготовка поверхности хромируемого изделия
Состоит из трёх этапов:
- Механическая очистка, шлифовка и полировка.
- Обезжиривание.
- Никелирование.
Особенностью хромирования является то, что оно, наоборот, подчёркивает все имеющиеся неровности, сколы и трещины на поверхности изделия. Поэтому с поверхности хромируемой детали предварительно должны быть удалены следы старой краски, ржавчина, сколы, трещины и прочие дефекты. Подготовка хромируемой поверхности состоит из следующих этапов:
- Пескоструйная обработка.
- Полировка мелкой шкуркой.
- Шлифовка мягкими материалами и полировочной пастой.
Для обезжиривания нельзя использовать бензин или Уайт Спирит. В противном случае будут проблемы с качеством хромирования. Оптимальный вариант — приготовить специальный раствор:
- Натр едкий: 150 гр/л;
- Сода, кальцинированная: 50 гр/л;
- Клей силикатный: 5 гр/л.
Раствор подогревается до 90 градусов. После этого в него опускают деталь и выдерживают 20−40 минут, в зависимости от площади и рельефа поверхности детали.
Никелирование является последним этапом подготовки детали к хромированию. Процесс никелировки производят в специальной гальванической ванне. Катодом в этом случае является металлический никель, а в качестве электролита выступает раствор серной кислоты и солей никеля.
Этапы хромирования
Непосредственно хромирование состоит из ряда последовательных этапов:
- Процесс начинается с поднимания температуры электролита в ванне до 50−54 градусов.
- Помещается хромируемая деталь с предварительным присоединением к ней катодного выхода.
- После этого выдерживают некоторое время, не подавая напряжения в систему. В течение этого времени температура детали и электролита должны выровняться.
- После подачи напряжения обрабатываемая деталь находится в растворе как минимум 20 минут. В некоторых случаях хромирование может продолжаться 2−3 часа. Всё решается в индивидуальном порядке в зависимости от размера детали и необходимых конечных характеристик хромированного покрытия.
- После окончания процесса деталь достаётся из раствора, промывается и помещается в сушильный шкаф на 2−3 часа.
В интернете очень много видеоуроков по гальванике, в частности, по хромированию металлов. Поэтому все детали этого процесса можно почерпнуть там.
Химическое меднение стальных деталей своими руками
Процесс меднения металлических изделий называется гальваностегией. Он основан на осаждении на поверхность деталей другого металла, растворимого в специальной жидкости.
Технология омеднения включает изготовление раствора и создание разноименных электродов. В процессе гальваностегии, ионы меди, растворенные в электролите, притягиваются отрицательным полюсом (обрабатываемая деталь) на свою поверхность.
Омеднение различных деталей в промышленных масштабах применяется не только, как конечный процесс обработки поверхности металлических изделий. Он может использоваться для подготовки деталей к следующей операции, например, никелированию, серебрению или хромированию изделий.
Эти металлы плохо осаждаются на поверхность стальных деталей, а на омедненную поверхность ложатся очень хорошо. В свою очередь медь, осевшая на стальные детали, держится прочно и способствует выравниванию различных дефектов на ее поверхности.
Гальваника медью в домашних условиях: общие сведения
С технической точки зрения обработка – это электрохимический процесс. В процессе всегда есть два «участника» анод+электролит (источник металла) и деталь.
Технология гальваники медью в домашних условиях достаточно проста. Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Среди основных этапов гальванического меднения в домашних условиях:
- Подготовка поверхности (механическая и химическая).
- Нанесение подслойного покрытия (если необходимо)
- Меднение в соответствующем исходному металлу электролите.
Для декоративного гальванического меднения подойдут электролиты матового и блестящего меднения. После нанесения слоя, можно обработать поверхность в электролитах серебра, золота никеля и т.д.
Различные типы меднения
Меднение в домашних условиях могут выполнять даже новички в этом направлении. Чтобы получить качественное покрытие необходимо изучить все нюансы процедуры. Она может проводиться по одной из 2 технологий:
- Погружение в электролит. Заготовка погружается в жидкость и подается электроток. Обычно, используется в тех ситуациях, когда ее габариты не значительны.
- Без погружения в раствор. Более сложный процесс, но позволяющий достигать лучшего качества обмедненных поверхностей.
Во всех случаях необходимо подведение электричества, которое активизирует вещество.
Оптимальный метод выбирается в соответствии с поставленной целью:
- Формирование защитных и декоративных покрытий. Зачастую происходит смешение с никелем, хромом и медью. Получаются прочные и надежные поверхности.
- Защита при цементировании.
- Реставрация изделий.
Рассмотрим подробнее каждый из вариантов.
Омеднение с помещением в электролит
Наиболее доступный способ обмеднения в быту. Необходимы:
- Небольшого размера пластинки из меди.
- Проволока для проведения тока.
- Источник тока.
- Устройство для регулирования и измерения тока.
- Чтобы растворить медь используется обыкновенный электролит, свободно продающийся или легко готовящийся своими руками. Для приготовления следует делать смесь серной кислоты с дистиллированной водой в пропорциях 3 к 100 миллилитрам. Нужная смесь получается после добавления в него 20 г медного купороса.
- Деталь следует очистить щеткой и наждачкой, чтобы удалить оксидную пленку.
- Провести обезжиривание раствором соды и промыть.
- Подготовленная емкость заполняется электролитическим раствором.
- В емкости размещаются 2 пластинки, подключенные к токопроводящей проволоке. Меж ними помещается деталь, которой предполагается омеднение. Нужно проверить полное закрытие смесью и пластинок, и заготовки.
- Затем пластины подключаются к плюсовому полюсу источника, а заготовка садится на минус. Предварительно желательно подключать амперметр и реостат. Выставить диапазон тока до 15 мА на 1см2 площади поверхности изделия.
- Выдержать в течение 20 минут.
- Выключается питание, заготовка извлекается из раствора. В итоге получается тонкое покрытие из меди. Продолжительность процесса оказывает влияние на толщину напыления. Благодаря технологии можно добиваться слоя до 300 мкм и более.
Метод возможно применять для обновления алюминиевых вещей, используемых в быту. Например, столовая утварь из алюминия после омеднения обретет вторую молодость.
Читать также: Виды розеток на кухне
Омеднение без помещения в раствор
Метод не предполагает залитие детали жидкостью. Он прекрасно подходит обработки цинковых или алюминиевых изделий.
- Необходим провод – многожильный, медный. Снять изоляцию. Одна сторона распушается, делая подобие кисточки. Можно сделать что-то вроде рукояти для большего комфорта в работе. Другой край провода подключается к положительному полюсу источника тока. Напряжение – не больше 6 Вольт.
- Вышеописанным методом подготавливается электролит с медным купоросом. Посуда может использоваться любого типа, но лучше подобрать ту, которая позволит беспроблемно погружать кисточку из провода. Обрабатываемая деталь очищается от загрязнений. После этого проводами садится на отрицательный полюс источника тока.
- Процедура проводится следующим образом. Распушенный край-кисточка время от времени помещается в раствор. Ей следует проводить вдоль заготовки, не прикасаясь к ней. Поверхность нужно смочить электролитическим раствором. Во время обработки за счет отрицательного заряда деталь будет подтягивать ионы меди, покрываясь ими.
Это меднение металла подойдет для габаритных вещей, которые затруднительно поместить в емкость.
Необходимые инструменты для меднения в домашних условиях
«Ингредиенты», без которых меднение не состоится, но которые реально подготовить в домашних условиях. Наши гальваники утверждают, что прежде всего, нужны:
- Источник постоянного тока.Выбирается в зависимости от размера изделия.
- Аноды. Анодные пластины выполняют несколько функций. В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
- Рабочий электролит. Кислотный, щелочной или пирофосфорный раствор. Состав электролита выбирается в зависимости от исходного металла. Необходимо помнить, что любой электролит не универсален и подойдет не для всех работ.
Физико-механические характеристики меди и сферы использования меднения
Плотность меди 8,96 г/см 3 , атомная масса 693,54, удельное электрическое сопротивление 1,68×10 -8 Ом×м, температура плавления +1083°С. На открытом воздухе в присутствии агрессивных химических соединении медь окисляется, при контакте с сернистыми соединениями покрывается пленкой сульфида меди темно-коричневого или серого оттенков. Под влиянием углекислоты и влаги пленка приобретает зеленый цвет, верхний слой состоит из гидрокарбонатов. Медь легко растворяется в растворе азотной кислоты, разбавленная серная кислота на химическое меднение негативного влияния почти не оказывает. Но наличие кислорода увеличивает скорость протекания химических реакций. При наличии открытых пор в покрытии образуется гальванопара, что нужно учитывать при меднении. Железо в этом случае является анодом, коррозионные процессы протекают очень интенсивно.
В связи с такими особенностями, процесс меднения в большинстве случаев должен завершаться дополнительной обработкой поверхностей. Покрытия шлифуются или полируются до зеркального блеска. Медь имеет высокую адгезию с различными металлами: алюминий, серебро, цинк, никель, свинец, хром и т. д. В связи с этими особенностями химическое меднение часто используется для создания подслоя при серебрении, никелировании, хромировании поверхностей деталей. Меднение получило широкое распространение в качестве метода эффективной защиты отдельных участков деталей от появления эффекта науглероживании при процессе цементации. В зависимости от назначения деталей или изделий гальваническое нанесение меди может иметь следующую толщину:
Толщина слоя меди на поверхности обрабатываемых деталей
Сравнительные показатели растворов
В процессе меднения используется большое количество специальных технологических растворов, разделяемых на две большие группы:
- Простой кислый электролит. Из простых применяется фторборатный, кремнефторидный, сульфатный, хлоридный и сульфамидный раствор.
- Комплексный электролит. Преимущественно щелочные, медь присутствует как положительно или отрицательно заряженные комплексные ионы.
График поляризационных кривых осаждения меди из различных типов электролитов
Процесс осаждения в кислых электролитах происходит при высокой плотности по току, они устойчивы, просты по химическому составу. Главными составляющими являются соответствующие кислоты и соли, осадки меди из них достаточно плотны и имеют крупнокристаллическую структуру. Недостатки – непосредственное меднение стали, цинковых сплавов и иных металлов происходит с более низким отрицательным потенциалом, чем медь.
Обработка деталей в комплексных электролитах выполняется за счет комплексных ионов, для них требуется высокая катодная поляризация. Выход по току меньше, что способствует более равномерному осаждению, структура мелкокристаллическая. Используются пирофосфатные, цианидные, аммонийные, триполифосфатные, цитратные и другие растворы.
Способность рассеивания электролитов для меднения
Простые кислые составы
- Сульфатные. Главные компоненты серная кислота и сульфат меди. Сернокислое соединение отличается невысокой электропроводимостью, для повышения параметра добавляется серная кислота. Выход меди по току достигает 100%, на катоде не выделяется водород. За счет повышения концентрации кислоты уменьшается растворимость сульфата, что понижает верхний предел максимально допустимой плотности тока.
Влияние содержания серной кислоты на электропроводность электролита
При перемешивании увеличивается концентрация медных ионов на катодном слое. При повышении температуры возрастает растворимость сульфата меди, электролит повышает кислотность, что приводит к получению мелкокристаллических осадков.
Для улучшения катодной поляризации в электролит добавляются поверхностно активные вещества. Дополнительно они уменьшают образование наростов на острых краях.
Режимы и состав сульфатных электролитов для меднения
Для образования блестящего покрытия используются аноды АМФ, не допускающие образование шлама, или аноды из особо чистой рафинированной меди.
Влияние концентрации меди на плотность тока с перемешиванием (1) и без перемешивания (2). Электролит фторборатный.
Для недопущения попадания шлама аноды помещаются в чехлы, изготовленные из кислотоустойчивого материала, дополнительно раствор постоянно фильтруется.
- Фторборатные. Отличаются высокой устойчивостью, гальваническое нанесение получается плотным и мелкокристаллическим, рассеивающие показатели такие же, как при сульфатном меднении. За счет большой растворимости увеличивается плотность тока, осаждать медь непосредственно на детали нельзя.
Состав и режим работы фторборатных электролитов
При непрерывном перемешивании допускается повышать плотность тока. Контроль технологически параметров меднения осуществляется измерением кислотности раствора. Для повышения качества меднения используется карбонат натрия, для понижения медный купорос.
- Нитратные. Электролит используется при гальванопластике, обеспечивает повышенное качество осадка.
Режимы и состав нитратных электролитов
- Цианидные. Условия обработки значительно отличаются от осаждения из кислых, в них медь существует в виде комплексных ионов, что заметно понижает ее активность. Увеличение плотности тока принуждает катодный потенциал резко смещаться в поле отрицательных значений. Но процесс меднения нельзя производить при увеличенной плотности тока в связи с тем, что выход меди может падать до нуля. Главными компонентами раствора являются свободный цианид натрия и комплексный цианид калия. Во время работы содержание меди понижается из-за недостаточной их растворимости.
- Пирофосфатные. Медные осадки имеют мелкокристаллическую структуру, гладкие, блестящие или полублестящие. Для улучшения качества обработки и повышения катодной и анодной плотностей может добавляться медный купорос. Катодный потенциал в пирофосфатных растворах имеет более отрицательные параметры, чем у кислотных.
Читать также: Воронение металла в домашних условиях лимонной кислотой
Режим и состав пирофосфатных электролитов
- Этилендиаминовые. Процесс меднения может осуществляться непосредственно по поверхности стали, при низких плотностях тока катодная поляризация достигает больших значений. Рассеивающие характеристики выше, чем у сульфатных, но ниже, чем имеет цианидный раствор.
Режим и состав этилендиаминовых электролитов
Загрузка и выгрузка деталей должна выполняться при минимальной силе тока, в первые 40–50 секунд дается толчок тока, в три раза превышающий рабочие значения меднения.
- Полиэтиленполиаминовые. Во время обработки деталей потенциалы смещаются в поле отрицательных значений, электролит применяется вместо цианидных.
Режим работы и составы полиэтиленполиаминовых электролитов
- Аммонийные. В состав входит аммиак, сульфат аммония и сульфат меди. При невысоких плотностях тока уменьшается выход по току, улучшение меднения осуществляется за счет добавления нитрата аммония. Осадки равномерные по толщине, плотные и полублестящие.
Режимы работы и состав аммонийного электролита
Без специальной обработки поверхностей медные осадки имеют недостаточную адгезию, причина – пассивирование стали раствором аммиака. Улучшение параметров покрытия достигается введением в раствор нитрата меди. Устройство ванны меднения Линейные параметры и конструктивные особенности должны отвечать требованиям ГОСТ 23738-85. Гальваническая ванна изготавливается из модифицированных особо устойчивых пластиков, конкретные марки подбираются с учетом параметров технологических процессов.
Ванна без кармана. Наиболее простая конструкция, применяется как в отдельности, так и на производственных линиях.
Ванна без кармана
Ванна с карманом. Обработка может выполняться с одновременными процессами удаления верхнего загрязненного слоя электролита.
Ванна с карманом
Конкретный выбор ванны меднения осуществляется в зависимости от особенностей предприятия, характеристик подлежащих меднению деталей и общих производственных мощностей.
Во время проектирования рассчитываются максимальные нагрузки с учетом объема раствора, длина, высота и ширина может изменяться по желанию заказчиков. При необходимости на ванны меднения устанавливается дополнительное оборудование и водопроводная арматура. За счет специальных механизмов улучшается качество процесса меднения. Используемые пластики адаптируются к химическому составу электролита и температурным режимам меднения.
Механическая подготовка поверхностей
Перед меднением с поверхности должна удаляться окалина, заусеницы и раковины. Качество обработки регламентируется положениями действующего ГОСТа 9.301-86. Конкретные параметры шероховатости устанавливаются в зависимости от назначения покрытия. После механической обработки деталей с поверхности должны быть удалены все дефекты, оказывающие негативное влияние на качество меднения. В обязательном порядке удаляется техническая смазка и эмульсия, металлическая стружка, продукты коррозионных процессов и пыль.
Подготовка к меднению производится при следующих технологических операциях:
- Шлифование. Верхний слой деталей снимается абразивными элементами, может быть тонким, декоративным или грубым.
- Полирование. Во время операции сглаживаются мельчайшие выступы, поверхность блестящая зеркальная.
- Крацевание. Для очистки поверхностей применяются металлические щетки.
- Галтовка. Детали обкатываются в специальных колоколах.
- Химическое и электрохимическое обезжиривание. Для обработки используют органические и неорганические растворы.
От качества предварительной подготовки поверхностей во многом зависит процесс меднения и физические показатели осадков.
В современном мире больше распространение получил медный сплав. Он наносится на поверхность для придания внешней привлекательности различных изделий. Меднение в домашних условиях зачастую проводится для существенного повышения показателя электропроводности. В некоторых случаях рассматриваемый процесс является промежуточной операцией, которая позволяет нанести другое вещество на поверхность.
Подготовка материала
Как правильно подготовить простой электролит меднения
Стоит отметить, что гальваника в домашних условиях медью сложна, потому что химические реактивы найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
- Дистиллированная вода (или бидистиллят).
- Медный купорос.
- Соляная или другая кислота.
Готовый раствор имеет яркий синий цвет, запаха нет. Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами, особенно в домашних условиях: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах, а также обязательно указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.
Подготовка материала для меднения в домашних условиях
Химическое меднение — это альтернатива электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды металла подвергаются очистке по-разному:
- Сталь. Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
- Медь и сплавы. Обезжиривание осуществляется едким натрием, нагретым предварительно до 40°, около 10 минут.
- Чугун. Для процесса обезжиривания нужен раствор, содержащий едкий натрий, жидкое стекло, карбонат натрия и фосфат натрия при нагревании до 90°.
- Вольфрам. Меднение вольфрама в домашних условиях начинается с чистки предмета от грязи и прочих дефектов наждачной бумагой.
Водные растворы для химического меднения.
Водные растворы для химического меднения.
Химическое меднение применяется, например, при изготовлении печатных плат для радиоэлектроники, в гальванопластике, для металлизации пластмасс, для двойного покрытия одних металлов другими. Термическая обработка для медных покрытий необходима.
Воду для химического меднения и при нанесении других покрытий берут дистиллированную, но можно использовать и конденсат из бытовых холодильников. Химреактивы подойдут как минимум чистые (обозначение на этикетке «Ч»).
Помним, что:
- чистая азотная кислота 1,4 г/см3 = 0,71 см3/г
- чистая серная кислота 1,84 г/см3 = 0,54 см3/г
- чистая соляная кислота 1,19 г/см3 = 0,84 см3/г
- чистая ортофосфорная кислота 1,7 г/см3 = 0,59 х см3/г
- чистая уксусная кислота 1,05 г/см3 =0,95 см3/г
Процесс кадмирования металлов и сплавов заключается в следующем.
- Обработанную деталь обезжиривают в одном из водных растворов,
- Затем деталь декапируют = обезжиривают и активируют в одном из перечисленных в данном разделе растворов.
- Для алюминия и его сплавов перед химическим меднением проводят еще одну, так называемую, цинкатную обработку. Ниже приведены растворы для цинкатной обработки.После цинкатной обработки детали промывают в воде и завешивают их в раствор для борокобальтирования.
- Меднение . Последовательность приготовления: все химреактивы растворяют в воде обязательно в эмалированной посуде. Затем раствор разогревают до рабочей температуры и завешивают детали в раствор.
- Повысить сцепление пленки покрытия с основным металлом помогает — термическая обработка = низкотемпературная диффузия — процесс заключается в нагреве омедненных деталей до температуры 400°С и выдержке их при этой температуре в течение 1 часа. Если покрываемые детали закалены (пружины, ножи, рыболовные крючки и т.п.), то при температуре 400°С они могут отпуститься, то есть потерять свое основное качество — твердость. В этом случае низкотемпературную диффузию проводят при температуре 270-300°С с выдержкой до 3 ч. Такая термообработка повышает и твердость покрытия.
Составы растворов для декапирования
| Составы растворов для декапирования стали | г/л | Температура раствора | Время обработки |
| Состав 1 : | |||
| Серная кислота | 30-50 | 20°С | 20-60 с |
| Состав 2: | |||
| Соляная кислота | 20-45 | 20°С | 15-40 с |
| Состав 3 : | |||
| Серная кислота | 50-80 | 20°С | 8- 10 с |
| Соляная кислота | 20-30 | ||
| Составы растворов для декапирования алюминия и его сплавов | —!— | Температура раствора | Время обработки |
| Состав 1 : | |||
| Азотная кислота 10-15% раствор (по объему) | 20°С | 5-15 с | |
Составы растворов для цинкатной обработки алюминия и литейных алюминиевых сплавов.
| Составы растворов для цинкатной обработки алюминия | г/л | Температура раствора | Время обработки |
| При подготовке раствора 1 и 2 сначала отдельно в половине воды растворяют едкий натр, в другой половине цинковую составляющую. Затем оба раствора сливают вместе. | |||
| Состав 1 : | |||
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 250 | 20°С | 3-5 с |
| Оксид цинка = окись цинка = цинковые белил= ZnO. | 55 | ||
| Состав 2 : | |||
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 120 | 20°С | 1,5-2 мин |
| Сульфат цинка = сернокислый цинк = ZnSO4 | 40 | ||
| Составы растворов для цинкатной обработки литейных алюминиевых сплавов | г/л | Температура раствора | Время обработки |
| Состав 1 : | |||
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 10 | 20°С | 2 мин |
| Оксид цинка = окись цинка = цинковые белил= ZnO. | 5 | ||
| Сегнетова соль кристаллогидрат = тетрагидрат двойной натриево-калиевой соли винной кислоты = NaKC4h5O6·4h3O = тартрат калия-натрия | 10 | ||
| Составы растворов для цинкатной обработки деформируемых алюминиевых сплавов | г/л | Температура раствора | Время обработки |
| Состав 1 : | |||
| Хлорид железа(III) = хлорное железо = FeCl3 (крисаллогидрат) | 1 | 25°С | 30-60 с |
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 525 | ||
| Оксид цинка = окись цинка = цинковые белил= ZnO. | 100 | ||
| Сегнетова соль кристаллогидрат = тетрагидрат двойной натриево-калиевой соли винной кислоты = NaKC4h5O6·4h3O = тартрат калия-натрия | 10 | ||
Составы растворов для меднения.
| Составы растворов для меднения | г/л | Температура раствора | Cкорость наращивания пленки |
| Состав 1 : | |||
| Сульфат меди (II) = сернокислая медь = CuSO4 | 10 | 15-25°С | 10 мкм/ч |
| Серная кислота | 10 | ||
| Состав 2 : | |||
| Битартрат калия = виннокислый (иногда кислый виннокислый) калий = KC4H5O6 = пищевая добавка E336ii | 150 | 15-25°С | 12 мкм/ч |
| Сульфат меди (II) = сернокислая медь = CuSO4 | 30 | ||
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 80 | ||
| Состав 3 : | |||
| Сульфат меди (II) = сернокислая медь = CuSO4 | 8-50 | 20°С | 8 мкм/ч |
| Серная кислота | 8-50 | ||
| Состав 4 : | |||
| Сульфат меди (II) = сернокислая медь = CuSO4 | 10-50 | 20°С | 10 мкм/ч |
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 10-30 | ||
| Сегнетова соль кристаллогидрат = тетрагидрат двойной натриево-калиевой соли винной кислоты = NaKC4h5O6·4h3O = тартрат калия-натрия = калий натрий виннокислый | 40-70 | ||
| Формалин = раствор, содержащий 40% формальдегида, 8% метилового спирта и 52% воды | 15-25 | ||
| Состав 5 : | |||
| Сульфат меди (II) = сернокислая медь = CuSO4 | 63 | 20°С | 15 мкм/ч |
| Битартрат калия = виннокислый (иногда кислый виннокислый) калий = KC4H5O6 = пищевая добавка E336ii | 115 | ||
| Кальцинированная сода = карбонат натрия = натрий углекислый . Химическая формула, Na2CO3 | 143 | ||
| Состав 6 : Этот раствор позволяет получать пленки с небольшим содержанием никеля. | |||
| Сульфат меди (II) = сернокислая медь = CuSO4 | 80-100 | 20°С | 10 мкм/ч |
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 80- 100 | ||
| Кальцинированная сода = карбонат натрия = натрий углекислый . Химическая формула, Na2CO3 | 25-30 | ||
| Хлористый никель = Никель (II) хлористый 6-водный = Никель хлорид гексагидрат = Хлорид никеля = Nickel (II) Chloride Hexahydrate = Nickel Chloride 6-aqueous = NiCl2*6h3O | 2-4 | ||
| Сегнетова соль кристаллогидрат = тетрагидрат двойной натриево-калиевой соли винной кислоты = NaKC4h5O6·4h3O = тартрат калия-натрия = калий натрий виннокислый | 150-180 | ||
| Формалин = раствор, содержащий 40% формальдегида, 8% метилового спирта и 52% воды | 30- 35 | ||
| Состав 7 : Этот раствор отличается большой стабильностью работы по времени и позволяет получить толстые пленки меди. | |||
| Сульфат меди (II) = сернокислая медь = CuSO4 | 25-35 | 18-25°С | 8 мкм/ч |
| Гидроксид натрия = каустическая сода = каустик = Едкий натр = едкая щёлочь. Химическая формула NaOH | 30-40 | ||
| Кальцинированная сода = карбонат натрия = натрий углекислый . Химическая формула, Na2CO3 | 20-30 | ||
| Динатриевая соль этилендиаминтетрауксусной кислоты = комплексон-III = трилон Б = Trilon B = хелатон III = ЭДТА = EDTA | 80-90 | ||
| Формалин = раствор, содержащий 40% формальдегида, 8% метилового спирта и 52% воды | 20-25 | ||
| Роданин = rhodanine = 2-Thioxothiazolidin-4-one = C3h4NOS2 | 0,003-0,005 | ||
| Красная кровяная соль = калий железосинеродистый = красное синькали = феррицианид калия = калия гексацианоферриат = K3(Fe(CN) 6) /желтая кровяная соль тоже пойдет/ | 0,1-0,15 | ||
Техника безопасности при меднении в домашних условиях
Несмотря на возможность гальваники в домашних условиях (меднения), процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому нужно неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью в домашних условиях – работайте только в нежилом, хорошо проветриваемом помещении. Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты при меднении в домашних условиях нужно:
- Постоянно быть в респираторе, чтобы обезопасить дыхательные пути. лучше всего использовать вытяжку.
- Защитить руки прочными прорезиненными перчатками.
- Надеть специальную форму или клеенчатый фартук, противоожоговую обувь.
- Не забыть очки для безопасности зрительных органов.
- Не приносить в помещение еду и питье.
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Гальваника в домашних условиях: меднение
Почему в гальванике столь востребована именно медь? Она имеет высокую адгезию (иными словами – сцепление) к самым разным материалам. Это значит, что она превосходно держится на изделиях из стали, вольфрама, не отлетая и не скалываясь.
Медь – красивый яркий металл, внешне напоминает самородки розово-красного оттенка. Материал проводит не только тепло, но и электрический ток – отсюда и высокий спрос в сфере электротехники и приборостроении. Однако чистую медь найти сложно. Чаще она поставляется с различными примесями.
Медные покрытия:
- Отличаются малым сопротивлением, что используется в электротехнике
- Скрывает мелкие недочеты поверхности.
- Быстро окисляется, что используют для получения эффекта «антик».
Технологий меднения существует две. Одна происходит путем погружения изделия в раствор электролиты (с подачей тока или без). Второй же способ – это метод селективного нанесения покрытия без погружения в раствор. Рассмотрим оба.
Метод погружения
В домашних условиях поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
Дальше:
- Анодную пластину (можно две) помещают в емкость, которую будем называть ванной. На аноды замыкают положительную клемму.
- Между анодами на любом удобном проводнике подвешивается деталь, к ней подводят отрицательный полюс от блока питания.
- Готовый раствор вливается в ванночку – при этом уровень покрытия должен быть выше, чем расположена деталь.
- После подключения электродов к источнику тока выставляют рабочий ток. Это примерно 1 А/кв.дм. покрытия.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Покрытие без погружения
Данный способ меднения имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшую толщину металла. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне. Порядок действий при гальваническом меднении в домашних условиях:
- Готовят «тампон» для нанесения покрытия. Берут медный проводник и наматывают кусок искусственной ткани (полиэстер подойдет).
- Противоположный конец проводника подсоединяют к положительной клемме источника напряжения.
- Электролитным раствором наполняют емкость – так удобнее окунать карандаш.
- Деталь аккуратно очищают и обезжиривают, а потом помещают в пустую ванночку. Там изделие подсоединяется к отрицательной клемме.
- Тампон смачивают в растворе. Затем им проводят по поверхности изделия, закрашивая ее постепенно.
Процесс длится до полного покрытия медным слоем изделия.
Способы меднения металлов
Существует два базовых метода, с помощью которых выполняют покрытие металлов медью: гальваническое и химическое меднение. В обоих случаях главным условием является применение электролита на основе медного купороса, но при химическом меднении осаждение меди происходит без использования электрического тока.
С помощью химического метода нельзя получить покрытия большой толщины, но оно проще, дешевле и может выполняться в крайне простых условиях. С помощью него легко получить тонкие декоративные пленки не только на металлах, но и на пластике, стекле, керамике и пр.
К примеру, химическое меднение стали происходит за несколько десятков секунд путем простого погружения в медный купорос.
Погружение в электролитный раствор
Оба метода могут применяться с полным погружением детали в раствор электролита. При гальваническом методе анионы меди отрываются от анода и движутся к катоду под воздействием электрического тока, а при химическом их движение происходит за счет разной электроотрицательности металлов.
Поэтому в первом случае при прочих равных условиях за одну и ту же единицу времени осаждается гораздо большее количество меди, но при этом затрачивается электрическая энергия.
Меднение алюминия рекомендуется производить только методом погружения, которое необходимо выполнять сразу после обезжиривания и травления в кислоте, иначе на его поверхности быстро образуется прочная оксидная пленка.
В видеоролике ниже подробно рассказывается об условиях, которые необходимо соблюдать для качественного меднения алюминия.
Без помещения в электролитный раствор
Меднение изделий без помещения их в емкость с электролитом производится как с использованием источника тока, так и без него. Выбор метода зависит от условий выполнения работ и оборудования, которым располагает домашний мастер.
В первом случае необходимо изготовить медную кисточку из обрезка кабеля с большим количеством мягких медных жил. Ее подсоединяют к плюсу источника, а минус подают на изделие. Затем, постоянно обмакивая кисточку в электролит, «красят» подготовленную поверхность, подбирая по ходу условия и скорость меднения.
Во втором варианте изделие просто покрывают раствором медного купороса с помощью малярной кисти, очищая и обмывая его после каждого слоя. Толщина обмеднения в этом случае будет небольшой и зависит от условий обработки и количества наложенных слоев.
Этот метод хорошо подходит для меднения стали, к которой медь «липнет» даже при условии не очень хорошей подготовки поверхности. А при нанесении таким способом медного купороса на поверхность алюминия достаточно сложно добиться устойчивого результата из-за его склонности к быстрому окислению.
Использование медного купороса
Одно из основных условий качественного меднения — это использование максимально чистого медного купороса. Поэтому данный реагент лучше приобретать в хозяйственных или специализированных магазинах в упаковках, на которых указано процентное содержание сернистого сульфата меди (не ниже 97–98%).
Если на медном купоросе садово-огородного назначения не указан состав, то для электролита он не годится, т. к. может содержать различные добавки, влияющие на гальванический процесс.
При приготовлении электролита в домашних условиях не следует применять сырую водопроводную воду, поскольку она содержит недопустимые при меднении соединения хлора. Перед использованием ее следует отстоять и прокипятить или же просто приобрести дистиллированную.
ПОСМОТРЕТЬ медный купорос на AliExpress →
Особенности гальванопластики в домашних условиях
Гальванопластика — это процесс нанесения меди на проводящую или непроводящую поверхность изделия с последующим снятием покрытия с негативной матрицы. Таким образом можно получить множество очень точных копий с одного изделия. При этом, есть условие: наращивание меди толщиной не менее 200 мкм, чтобы изделие получилось прочным.
Важно учесть, что, если поверхность изделия не имеет свойств проводника, то потребуется больше усилий – а именно, особое предварительное покрытие графитом, серебром или медью. Основным металлом для осуществления гальванопластики считается медь, но можно выращивать матрицы из серебра чистотой 9999.
Обучение гальванике
Можно сделать вывод, что меднение сегодня — это один из наиболее актуальных гальванотехнических процессов, обучиться которому может каждый. проводит обучение по направлению «Гальваника» для всех желающих! Вы сможете выбрать удобную для Вас программу обучения, которая лучше всего подойдет для гальваники в домашних условиях и не только. Все интересующие вопросы можно задать по телефону или по электронной почте, наши технологи проконсультируют по курсам для обучения.
Видео руководство по меднению деталей в домашних условиях:
Подробности Вы можете узнать по ссылке:
Гордиенко Анастасия Вадимовна Автор материалов Должность: главный технолог ООО «6 микрон» Образование: высшее Опыт работы в гальванике: 11 лет
Можете ли вы гальванизировать медь пищевой содой? Новичок
Традиционно люди, занимающиеся гальванопокрытием, используют уксус вместе с дистиллированной водой для приготовления электролитного раствора меди.
После того, как раствор электролита будет готов, вы можете нанести покрытие на желаемую деталь. Однако это не единственный способ сделать это, и электролиты можно приготовить и с помощью пищевой соды.
Ответ на вопрос Можно ли гальванизировать медь пищевой содой ?
На медную пластину с помощью пищевой соды (также известной как карбонат натрия) добавьте пищевую соду в дистиллированной воде в банке.
Возьмите два куска меди и окуните одну сторону в раствор пищевой соды и воды, а другие стороны подключите к источнику питания (источнику питания 1 AMP).
После соединения одного куска меди с положительным проводом, а другого с отрицательным проводом (шина), ионы меди растворятся в растворе.
Это создаст раствор синего медного электролита, который вы затем можете использовать для покрытия вашего изделия.
КАКОВА ПРАВИЛЬНАЯ ПОДГОТОВКА ПЕРЕД ГАЛЬВАНИРОВКОЙ ВАШЕГО ИЗДЕЛИЯ?
Каждая деталь, на которую будет нанесено гальваническое покрытие, нуждается в надлежащей подготовке, прежде чем она будет готова к гальваническому покрытию.
При неправильной подготовке процесс покрытия не проходит гладко; в частности, невозможно добиться однородного покрытия.
Подготовка перед гальванопокрытием делится на два этапа, первый из которых – приготовление раствора электролита.
Необходимо дать время для приготовления раствора, пока медный кусочек не растворится в растворе должным образом.
Вторым этапом подготовки является полная очистка детали, на которую наносится гальваническое покрытие.
Его следует хорошо протереть и очистить, чтобы на нем не осталось грязи, жира с кожи или любых других частиц.
ПРОЦЕСС ИЗГОТОВЛЕНИЯ МЕДНОЙ ПЛИТЫ С ПИЩЕВОЙ СОДОЙ?
Это не очень сложный процесс, и, поскольку я документирую свой опыт гальваники и гальванопластики, вот чему я научился.
СОБЕРИТЕ НЕОБХОДИМЫЕ МАТЕРИАЛЫ.
Для настройки системы покрытия вам потребуется дистиллированная вода, пищевая сода, источник питания постоянного тока, два зажима типа «крокодил», два куска медного металла, кусок, который вы пытаетесь покрыть металлом, и контейнер, который подходит для металла. Вы хотите, чтобы гальваническое покрытие было погружено в воду.
Все эти предметы можно легко найти в местном оборудовании или даже у себя дома.
Блок питания имеет два контакта, которые облегчают процесс, но вы также можете использовать блок питания с более низким напряжением.
Зажимы типа «крокодил» представляют собой стандартные изолированные электрические провода с металлическими зажимами на концах, используемые для соединения двух цепей.
Кусок меди является источником ионов, которые превращают раствор для гальванопластики в гальваническое покрытие.
Никель и сталь — это два металла, которые можно легко покрыть медью, но вы также можете попробовать другие металлы.Вы также можете электроформовать органические вещества, пластиковую смолу и т. д. с помощью проводящей краски.
ИСПОЛЬЗУЙТЕ СООТВЕТСТВУЮЩИЕ ЗАЩИТНЫЕ СРЕДСТВА
Крайне важно, особенно в этом случае, вы занимаетесь гальванопокрытием в качестве хобби у себя дома, что увеличивает риск.
При нанесении гальванических покрытий на различные металлы важно помнить, что вы имеете дело с кислотами и другими опасными химическими веществами, от которых вам необходимо защищаться.
Носите перчатки, защитные очки и лабораторные халаты или одежду, которую не жалко испортить, если что-то брызнет во время процесса.
ЧИСТКА МЕТАЛЛИЧЕСКОЙ ПОВЕРХНОСТИ
Чтобы получить ровный гальванический слой на изделии, необходимо сначала тщательно очистить поверхность изделия.
Грязь и масла на поверхности изделия могут помешать металлу-донору равномерно покрыть поверхность. Начните с обезжиривающего средства, такого как моющее средство (средство для мытья посуды), а затем обязательно протрите металл абразивным или кислотным очистителем, чтобы поверхность была чистой.
ПОДГОТОВКА ЭЛЕКТРОЛИТА
Этот процесс уже был объяснен в статье, но вот подробное объяснение.Чтобы сделать раствор электролита, вы должны смешать пять частей дистиллированной воды с 1 частью пищевой соды.
Источник питания предназначен для получения тока, необходимого для приготовления электролита.
Прикрепите один кусок металла к одному контакту, а второй — ко второму контакту источника питания.
На данном этапе не имеет значения, какая часть меди к какой клемме подключена, просто к каждой части меди прикрепляется отдельный зажим.
После того, как вы включите медные детали, погруженные в раствор, вы начнете замечать, что цвет раствора станет синим.
Это будет ваш раствор медного электролита, который вы затем сможете использовать для металлизации вашего изделия.
СОЕДИНИТЕ ВАШ ИЗДЕЛИЕ С МЕДНЫМ ПРОВОДОМ И ПОКРЫТИЕМ ЗВЕЗДОЙ
Подсоедините положительный провод источника питания к куску меди, погруженному в раствор, это анод, а затем подсоедините отрицательный провод к катоду (шине) к нужному элементу. гальванизировать.
После того, как вы подключите кабели к источнику питания, вы заметите, что ваша деталь со временем покрывается металлом.
Однако здесь важно понимать, что если подключить провода обратным вышеописанным способом, то процесс металлизации не произойдет.
Итак, подключите положительный провод к куску меди (анод), а отрицательный провод (катод) подключите через вашу (шину) к куску, который вы покрываете.
ВОЗМОЖНО ЛИ ВЫПОЛНЯТЬ ЭЛЕКТРОПОКРЫТИЕ НЕСКОЛЬКИХ ИЗДЕЛИЙ ОДНОВРЕМЕННО?
Процесс металлизации одной детали более доступен и менее сложен, как вы можете видеть на шагах, описанных выше.
Но как насчет того, чтобы одновременно покрыть два или более куска – возможно ли это? Даже очень.
Вы можете гальванизировать несколько деталей одновременно; однако он потребует дополнительного ухода.
Вам придется разделить отрицательный провод (шину) источника питания на несколько частей и соединить каждую часть с частями, которые вы собираетесь гальванизировать.
Это замедлит процесс, но в конечном итоге вы получите несколько деталей одновременно.
КАКОВЫ ПРИМЕНЕНИЕ/НАЗНАЧЕНИЕ ГАЛЬВАНИЧЕСКОГО ПОКРЫТИЯ В ИЗГОТОВЛЕНИИ ЮВЕЛИРНЫХ ИЗДЕЛИЙ?
Люди различных ремесел используют золочение, но больше других им пользуются ювелиры.
Благодаря тому, что покрытие предлагает ювелирам, это не очень дорогой вариант.
Гальваническое покрытие улучшает внешний вид и однородность цвета ювелирных изделий.
Например, вы можете взять медное украшение, которое вы гальванопластикой, и нанести на него гальваническим способом серебро. Это придаст готовому изделию новый вид серебра.
Процесс гальванического покрытия обычно улучшает устойчивость ювелирных изделий к потускнению, что означает, что ювелирные изделия будут оставаться полированными и красивыми в течение длительного периода времени.
Используется на недрагоценных металлах, таких как серебряные ювелирные изделия, для придания им золотого вида и на медных изделиях после гальванопластики, чтобы придать им серебряный вид.
КАКОВЫ ПРЕИМУЩЕСТВА И НЕДОСТАТКИ ГАЛЬВАНИЧЕСКОГО ПОКРЫТИЯ?
Гальваническое покрытие имеет несколько преимуществ, в первую очередь устойчивость к коррозии.
Склонное к коррозии вещество, такое как металлы, может быть покрыто слоем неагрессивного материала, тем самым защищая исходные металлы от коррозии.
Кроме того, тусклым поверхностям можно придать блеск и блеск с помощью гальванического покрытия, тем самым украсив их.
Аналогичным образом, некоторые из недостатков гальванического покрытия заключаются в проблемах с утилизацией отходов, образующихся в процессе, поэтому важно проконсультироваться с местными властями для получения инструкций по утилизации.
Кроме того, этот процесс требует многократного нанесения покрытия на металл, что иногда требует много времени и средств.
ПОСЛЕДНИЕ МЫСЛИ
Процесс гальваники с помощью пищевой соды широко используется людьми, занимающимися гальванопокрытием в качестве хобби дома.
Это более простое и практичное решение для деталей, которые вы хотите гальванизировать. Теперь, следуя шагам, описанным выше, вы можете гальванизировать свои изделия в домашних условиях с помощью пищевой соды.
Теперь вы знаете, что можно гальванизировать медь пищевой содой?
ИСТОЧНИКИ:
https://www.chemistry.stackexchange.com/questions/13902/can-i-perform-electroplating-with-sodium-carbonate-and-med
https://www.instructables.com /Высококачественное меднение/
https://www.pinterest.co.uk/amp/pin/420594052697173496/
Химия своими руками: научитесь гальванике
Адам Гольфер
Когда вы видите тонкий слой металла — на чем угодно, от хромированных автомобильных деталей до сверл и ювелирных изделий — вероятно, это гальваническое покрытие.Процесс прост: подайте ток через раствор соли металла, чтобы покрыть проводящую поверхность ионами металла. В этом проекте мы покрываем графит (в виде карандашного рисунка) медью, материалом для электропроводки. Это превращает изображение в схему, которая может питать светодиод. Новый способ подключить ваш дом? Нет. Круто? Определенно.Расходные материалы
• Сульфат меди (например, Zep Root Kill)
• Белый уксус
• Пластиковая соломинка
• Прозрачная пленка
• Наждачная бумага, лента
• №2 карандаша
• 9-вольтовая батарея
• № 2 грифеля механического карандаша
• Два набора разъемов типа «крокодил»
• Светодиод с подключенным резистором
1. В прозрачной миске смешайте 3 столовые ложки сульфата меди с 1 стаканом белого уксуса. Перемешайте соломинкой. Когда уксус станет синим, медь растворится.
2. Используйте мелкую наждачную бумагу, чтобы придать шероховатость куску прозрачной пленки.
3. Нанесите изображение на поцарапанную пленку номером2 карандаш. Ваше изображение должно состоять из одной толстой линии и доходить до края пленки.
4. Закрепите красный зажим типа «крокодил» на положительной клемме 9-вольтовой батареи. Закрепите другой красный зажим на механическом графите карандаша.
5. Закрепите черный зажим типа «крокодил» на отрицательной клемме аккумулятора. Прикрепите другой черный зажим к краю вашего рисунка.
6. Не допуская контакта зажима типа «крокодил» с жидкостью, погрузите пленку в чашу.Прикрепите зажим к краю чаши.
7. Погрузите грифель карандаша в раствор. Прикрепите зажим «крокодил» к миске. Растворенная медь ляжет на ваш рисунок. (Вы увидите, как на проводе образуются пузыри.)
8. Когда рисунок полностью покроется медью, отсоедините зажимы от аккумулятора и высушите рисунок бумажным полотенцем.
9. Проверьте медь с помощью двух отдельных чертежей с покрытием. Подсоедините один рисунок к положительной клемме аккумулятора с помощью зажима типа «крокодил», а другой — к отрицательной клемме с помощью второго зажима.Прикоснитесь одной ножкой светодиода к каждому рисунку; да будет свет!
Сара Хансен преподает химию в Колумбийском университете и исследует образование в области химии в педагогическом колледже Колумбийского университета.
Этот контент создается и поддерживается третьей стороной и импортируется на эту страницу, чтобы помочь пользователям указать свои адреса электронной почты. Вы можете найти дополнительную информацию об этом и подобном контенте на сайте piano.io.
High-Speed Bright Copper Electroplating Solution —
Упаковка
1-литровая полиэтиленовая бутылка, 1-галлонное или 5-галлонное ведро, отвечающее требованиям ООН, если не указано иное.
Качество и характеристики отложений
- Плотность 8,9 г/см3
- Удельное электрическое сопротивление 1,7 – 1,8 мкОм·см
- Высокая чистота пленки (<10 ppm для N, S, C, Cl)
- Низкая шероховатость поверхности , RMS < 10 нм при толщине меди 1 мкм
- Планаризация канавок (отсутствие выемок в канавках шириной 1 мкм и глубиной 0,5 мкм с толщиной меди 0,8 мкм)
- Сильная (111) текстура с небольшими (220) и (200)
- Коэффициент отражения > 75 %
- Удлинение 19–32 %
Особенности и преимущества
- Использование одного гальванического раствора, содержащего гальванические добавки
- Стабильные добавки с большим технологическим окном 7 9038 2 электролит высокой чистоты и длительный срок хранения Высокая температура помутнения (> 80 C) и низкое пенообразование
- Ванна для гальваники с низким поверхностным натяжением (~44 дин/см при 25 C)
- Высокоскоростное гальванопокрытие (>4 мкм/мин)
- Равномерные и плоские выпуклости, подушечки, узоры и перераспределения слоев 902 38
- Заполнение сквозных отверстий и канавок без пустот
Общее описание
Высокоскоростной раствор для гальванопокрытия меди представляет собой электролитно-кислотный медный процесс, разработанный для покрытия медных выступов, столбов, прокладок, шаблонов и перераспределяющих слоев, а также для заполнения переходных отверстий и траншей на широкий выбор подложек, включая полупроводники, стекло, полимеры и др.Процесс высокоскоростного гальванопокрытия меди NANO3D работает в широком диапазоне плотностей тока и обеспечивает превосходную метательную способность, улучшенные характеристики выравнивания и пластичные отложения с низким напряжением. Процессы гальванопокрытия меди NANO3D дают блестящие медные отложения и гладкую поверхность. Раствор для гальваники меди NANO3D состоит из сульфата меди и серной кислоты с небольшими добавками соляной кислоты и органических добавок. Органические добавки NANO3D имеют широкое окно процесса концентрации, что устраняет необходимость в отдельных растворах добавок и пополнении примерно на 120 ампер-часов гальванического покрытия.
Советы и советы по гальванике
Этот раздел будет содержать полезные немного информации о гальванике и общей реставрации. Они расположены в алфавитном порядке.
Если у вас есть хорошие советы и трюки, пожалуйста, свяжитесь с нами, и мы добавим их ниже.
Активация:
Активация металлической поверхности до нанесения покрытия является одной из наиболее важных частей процесса покрытия и часто упускается из виду!
Активация — удаление оксидный слой, который образуется на поверхности металла стандартным кислотным металлом химическая реакция, при которой ионы водорода отбирают электроны у оксидов металлов с образованием водород и соли металлов.
Процесс активации, который на основе кислотной активации или кислотного травления‚ также удалит любое щелочное мыло которые остаются на поверхности после процесса щелочной очистки. Оба щелочные мыла и оксиды вызывают окрашивание и могут вызвать пропуск покрытия, расслаивание и образование пузырей.
Мягкие металлы, такие как цинк, медь, бронза и латунь легко активируются простым травлением или кислотой активации, такие как наши сухие кислотные травильные соли. При активации мягких металлов‚ особенно важно промывать очень хорошо после процесса кислотного травления, чтобы удалить все следы кислоты.Если полоскание не тщательное, окрашивание будет видно, как правило, на края предмета.
Более твердые металлы, такие как нержавеющая сталь, никель, копия хрома и сталь, также можно активировать кислотным травлением, но время погружения будет больше, а концентрация огурец будет выше.
Еще один способ активировать некоторые из более твердые металлы — использовать процесс обращения тока после кислотного травления. Это делается путем изменения полярности в резервуаре для покрытия на 30 секунд. до нанесения покрытия.Металлы, которые выигрывают от этого типа активации, — это никель‚ Реплика из хрома и нержавеющей стали. При использовании текущего процесса реверсирования‚ изделия должны быть протравлены и хорошо промыты перед тем, как отправиться в гальванический резервуар. Делать не используйте этот тип активации дольше 30 секунд!
Перемешивание — еще одна важная часть процесса покрытия, которая часто упускают из виду домашние тарелки. Верно сказать, что для мелких деталей вы можете часто все еще получают хорошие результаты без него, но в целом наличие агитации повысит качество конечных результатов.Агитация помогает при удалении материалов с поверхности металла, увеличивая потенциал электрода, делая покрытие более эффективен, а также помогает предотвратить накопление загрязнений на поверхности слой.
Цинкование дает лучшее результаты при перемешивании, но все типы покрытия резервуаров выиграют от некоторых форма агитации во время покрытия. При использовании перемешивания во время меднения убедитесь, что ваши аноды завернуты или помещены в пакеты для анодов. Растворение медных анодов приводит к тому, что более крупные частицы оседают в электролите, без анодных мешков и при перемешивании эти частицы будут осаждаться на ваших предметах, вызывая матовую и зернистую поверхность.
Существует два основных метода, могут быть использованы, воздушные и механические.
- Воздушный – один из самых дешевых способов для взбалтывания электролита во время нанесения покрытия. Самый простой способ использовать воздух для агитации использовать небольшой воздушный насос и пластиковую трубку. Небольшое количество кремния будет удерживать пластиковую трубку на дне бака. Тебе понадобится чтобы опорожнить и очистить резервуар, прежде чем вы сможете установить силиконовую трубку на место. Для больших резервуаров или если больше воздуха необходимо перемешивание, тогда вам понадобится более мощный насос.И снова аквариум насосы можно купить разных размеров с разным уровнем подачи воздуха и Вы можете добавить к этому воздушный камень, чтобы получить много волнений. если ты хотите сделать свою собственную пузырьковую стену из воздушной трубки, затем заблокируйте конец воздушную трубку и просверлите в ней несколько отверстий диаметром 2 мм рядом с заблокированным концом примерно на 1 см. отдельно. Проверьте его в миске с водой, чтобы увидеть, нужно ли вам больше отверстий.
- Механическое перемешивание также может используется и может быть таким же простым, как перемешивание электролита во время нанесения покрытия.Это хорошо при выполнении декоративной тарелки на 15 минут но когда нужна толстая тарелка тогда стоять и перемешивать в течение часа нецелесообразно! Вместо этого аквариум Можно использовать фильтр-насос. Это не воздушный тип; этот тип использует небольшой электродвигатель с крыльчаткой для создания потока воды. Эти насосы нужны быть погруженным в электролит для работы.
Это отличная техника, которую можно использовать для покрытия мелких предметов, а также использоваться для ремонта предметов, которые не могут быть легко разобраны.Идеально подарить тонкие декоративные покрытия, но могут быть использованы для получения более толстых покрытий, если они используются для дольше. Его также можно использовать для покрытия только определенных областей, поэтому, если вы пытаетесь создавать изношенные участки на определенных элементах, таких как шейки подшипников или корпуса.
Некоторые моменты, о которых следует помнить:
- медленнее, чем покрытие резервуара
- не так легко наносить толстые пластины
- выравнивание пластины не так хорошо из-за отсутствие выравнивателей и уменьшенная толщина плиты, поэтому поверхность нуждается лучше подготовиться
- сменные растворы необходимы при нанесении кистью много.
Очистка:
Очистка является наиболее важным этапом гальваники. Это критично в достижения хорошего качества покрытия и обеспечения того, чтобы электролит оставался в отличное состояние.
Крайне важно, чтобы очистка тщательно и что предметы, подлежащие покрытию, должны быть очень чистыми. Помните всегда надевать перчатки и следить за их чистотой, чтобы не переносить и виды загрязнений, в основном жир с рук, на вашу сторону.
Есть несколько основных шагов, когда зачистка деталей под гальванику. Имейте в виду, что для сильно изношенные или изрытые предметы с большим количеством масла и смазки на поверхности.
1. Механическая уборка
2. Щелочные чистящие средства
3. Clinse
4. Кислотный очиститель
5. Rinse
6. Тест на чистоту
6. Активация
8. РАБИЧЕНИЯ
9. РАЗМЕЩЕНИЕ
Механическая очистка включает песок пескоструйная обработка, полировка, полировка и т.и может быть быстро и легко. Цель состоит в том, чтобы удалите любые следы ржавчины, краски или грязи.
Щелочная очистка используется для удаляют множество различных загрязнений, в основном тяжелые масла и жиры. Его можно использовать либо как очиститель для замачивания, когда деталь погружается в очиститель, либо как электро очиститель.
Кислотная очистка удалит любые оставшиеся оксиды, а также некоторые легкие почвы.
После завершения первого часть процесса очистки, важно проверить чистоту поверхности перед активацией.Тест на разрыв воды — это простой и быстрый способ проверки. Просто окунуться в чистую воду и посмотрите, не покрылась ли вещь водяной пленкой или на ней образовались пузыри. Если на нем есть водяная пленка без валиков, то он может перейти в стадия маринования. Если вы видите капли воды, значит, вам нужно умыться. моющее средство и воду, хорошо прополощите и повторите испытание на разрыв водой еще раз, пока оно не проходит. Вы также можете использовать тест белой ткани. Просто протрите часть белой тряпкой, чтобы проверить наличие следов на поверхности.Если ткань не остается белый вам нужно будет повторить процессы очистки перед активацией.
Активация критична в гарантируя, что новая поверхность прилипнет к основному металлу и создаст хорошую связь. То активационная кислота слегка травит поверхность, удаляя оксиды и металл с поверхность, чтобы обнажить атомы чистого металла. Наш сухой кислотный рассол специально разработан для использования в качестве протравки для покрытия или в качестве активатора металла. Вы также можете используйте соляную кислоту в концентрации от 5% до 20%.Серная кислота также может использоваться для некоторых металлов в концентрациях от 1% до 10%.
После маринования и промывки вам потребуется сразу на тарелку. Таким образом, вы не дадите металлу времени сформироваться. оксидный слой на поверхности.
Чем лучше вы сможете приготовить поверхности, тем лучше будут результаты. Итак, потратьте дополнительное время на сглаживание, полировку и полировка при необходимости. Это важно при нанесении покрытия кистью, поскольку вы только положить очень тонкую пластину на основной металл, чтобы получить более полированный основной металл лучше.При полировке или полировке не забудьте снять при необходимости отполируйте пленку растворяющим очистителем и промойте моющим средством и водой снова после. Всегда проверяйте тест на разрыв водой перед травлением.
Подумайте об инвестировании на скамейке буфер/измельчитель. Количество времени и усилий, которое это сэкономит, сделает это стоит своих денег.
Помните, что чистота рядом с благочестие, так что если вы хотите быть богом гальванопокрытий, то чистите, чистите и еще раз чистите!
Для получения дополнительной информации см. на нашу страницу очистки.
Электролит:
Содержание электролита в чистоте очень важно, так как это продлевает срок службы электролита и обеспечить высокое качество покрытия. Если вы столкнулись с какими-либо проблемами при нанесении покрытия первое, что нужно сделать, это сделать тестовую пластину. Это делается подготовка 2-дюймового куска медной водопроводной трубы. Очистите тонкой проволочной ватой, пока блестящий, затем стирайте в моющем средстве и воде, пока он не пройдет тест на разрыв водой. Убедитесь, что бак готов к покрытию, поэтому нагрейте его до температуры и включите перемешивание.Тарелка при слабом токе, поэтому при использовании регулятора тока все провода сопротивления в цепи. При использовании плиты с переменным питанием на 0,3 ампера. Тарелка для 20 минут. Если покрытие матовое, то, согласно нашему руководству, добавьте немного ухода. отбеливатель и повторите попытку. Если все еще тускло, то профильтруйте электролит через фильтровальная бумага для кофе и фиктивный электролит (сделать тарелку) добавить немного больше поддерживающего отбеливателя и повторите попытку.
Охрупчивание:
Водородное охрупчивание может быть вызвано электроочисткой, гальванопокрытием и травлением.Это может вызвать проблемы с высокопрочными деталями, делая их хрупкими и склонными к поломке. отказ при стрессе.
Существует несколько способов уменьшить Эта проблема; механическую очистку изделия, а не электроочистку, используйте щелочные чистящие средства, нагретые для сокращения времени погружения, убедитесь, что промывка тщательная, а если промывка бака, убедитесь, что вода очистите, уменьшите время травления до 60 секунд и, по возможности, сократите покрытие токи и время покрытия.
После покрытия (и перед пассивацией) выпекать изделия в духовке при температуре около 190-220°С на 1-2 часа.
Температура электролита:
пришло время рассмотреть какую-либо форму нагрева бака. Все гальванические электролиты выгоду от нагрева бака в той или иной форме. Простые способы нагреть резервуары таковы: следующим образом:
Для небольших резервуаров
1. Поместите резервуар в емкость с кипятка и подождите, пока они нагреются.
2. Наполните пластиковую бутылку кипятка и поместите внутрь бака, стараясь не переполнить бак.
3. Поместите резервуар на нагревательный мат. обычно для более низких температур покрытия, но все же будет повышать температуру. Убедитесь, что вы делаете это только со стеклянным или металлическим резервуаром — пластик деформироваться и может расплавиться.
4. Термостатические нагреватели самый простой способ, так как вы можете предварительно установить температуру и оставить ее нагреваться. Не забудьте дать ему несколько часов от холода, чтобы достичь правильной температуры.
Для больших резервуаров
1. Термостатические нагреватели лучший метод для больших резервуаров.
2. Иногда требуется перемешивание горячего воздуха. используется в очень больших резервуарах.
3. Комбинированный нагрев и фильтрация также используются системы.
4. Рубашки бака с подогревом.
После достижения температуры процесс покрытия будет держать резервуар в тепле или если покрытие будет выполнено непрерывно тогда это может быть случай охлаждения бака, если он становится слишком горячим!
Температурные диапазоны для наших гальванические электролиты:
Металл | Диапазон (°C) | Идеально (°C) |
Цинк | 15 – 40 | 25 – 30 |
Медь | 15 – 50 | 25 – 40 |
Никель/ Реплика Хром | 30 – 50 | 30 – 50 |
Латунь/бронза | 20 – 40 | 25 – 40 |
Кобальт | 30 – 50 | 35 – 50 |
Гальваническое покрытие 101: Как работает гальваническое покрытие металлов
Гальваническое покрытие позволяет сочетать прочность, электропроводность, стойкость к истиранию и коррозии, а также внешний вид определенных металлов с различными материалами, имеющими свои преимущества, такими как доступные по цене и/или легкие металлы. или пластики.
Из этого руководства вы узнаете, почему многие инженеры, исследователи и художники используют гальваническое покрытие на каждом этапе производства — от прототипирования до массового производства.
Информационный документЧитайте дальше, чтобы узнать, как инженеры добавляют металл к 3D-печати из смолы и почему гибридные металлические детали могут открывать двери для удивительного диапазона применений, включая (но не ограничиваясь) прочность и долговечность конечного использования.
Загрузить информационный документГальваника — это процесс использования электроосаждения для покрытия объекта слоем металла.Инженеры используют контролируемый электролиз для переноса желаемого металлического покрытия с анода (часть, содержащая металл, который будет использоваться в качестве покрытия) на катод (часть, на которую будет нанесено покрытие).
Схема гальванического покрытия медью с использованием электролитной ванны из сульфата меди, серной кислоты и ионов хлора. (источник изображения)
Анод и катод помещаются в химическую ванну с электролитом и подвергаются непрерывному электрическому заряду. Электричество заставляет отрицательно заряженные ионы (анионы) двигаться к аноду, а положительно заряженные ионы (катионы) — к катоду, покрывая или покрывая желаемую часть ровным металлическим покрытием.При гальваническом покрытии используется материал подложки (часто более легкий и/или более дешевый материал) и герметизируется подложка в тонкой оболочке из металла, такого как никель или медь.
Гальваническое покрытие чаще всего применяется к другим металлам из-за основного требования, чтобы основной материал (подложка) был проводящим. Хотя они менее распространены, были разработаны автокаталитические предварительные покрытия, которые создают ультратонкий проводящий интерфейс, позволяющий наносить различные металлы, в первую очередь медные и никелевые сплавы, на пластиковые детали.
Гальваническое покрытие и гальванопластика выполняются с использованием электроосаждения. Разница в том, что при гальванопластике используется форма, которую удаляют после формирования детали. Гальванопластика используется для создания цельных металлических деталей, тогда как гальваническое покрытие используется для покрытия существующей детали (изготовленной из другого материала) металлом.
Вы можете гальванизировать один металл на предмет или комбинацию металлов. Многие производители предпочитают наносить слои металлов, таких как медь и никель, чтобы максимизировать прочность и проводимость.Материалы, обычно используемые в гальванике, включают:
- Латунь
- Кадмий
- Хром
- Медь
- Золото
- Железо
- Никель
- Серебро
- Титан
- Цинк
Подложки могут быть изготовлены практически из любого материала, от нержавеющей стали и других металлов до пластика. Ремесленники гальванопокрывали органические материалы, такие как цветы, а также ленты из мягкой ткани.
Важно отметить, что непроводящие подложки, такие как пластик, дерево или стекло, необходимо сначала сделать проводящими, прежде чем на них можно будет наносить гальваническое покрытие.Это можно сделать, покрыв непроводящую подложку слоем токопроводящей краски или аэрозолем.
Благодаря научным достижениям в области производства материалов и пластмасс легкие и недорогие пластмассовые детали заменили более дорогие металлические детали в самых разных областях применения, обслуживающих различные отрасли промышленности, от автомобилей до водопроводных труб.
Хотя пластик имеет ряд преимуществ перед металлом, во многих случаях металл по-прежнему доминирует. Как бы вы ни старались, вы никогда не получите пластик с такой же роскошной отделкой, как у меди.И хотя пластик может быть более гибким, чем большинство металлов, он не такой прочный. Здесь на помощь приходит металлическое покрытие.
3D-печать предлагает уникальные преимущества в сочетании с гальванопокрытием. Инженеры часто выбирают подложки для 3D-печати из-за свободы проектирования аддитивного производства. Часто гальванопокрытие 3D-печатных деталей дешевле, чем литье, машинная обработка или использование других методов производства, особенно когда речь идет о прототипировании.
Стереолитография (SLA) 3D-печать идеально подходит для гальванопокрытий, поскольку позволяет создавать 3D-печатные детали с очень гладкими или тонко текстурированными поверхностями, которые делают переход между двумя материалами — пластиком и металлом — бесшовным.Он также создает водонепроницаемые детали, которые не будут повреждены при погружении в химическую ванну, необходимую в процессе гальванического покрытия.
С инженерной точки зрения сочетание 3D-печати и гальванического покрытия предлагает уникальные варианты прочности на растяжение для готовых конструкций. Как вы можете видеть на диаграмме выше, сочетание этих двух производственных процессов устраняет разрыв в прочности на растяжение между двумя группами материалов.
Металлическое покрытие может сильно повлиять на механические характеристики пластиковых деталей (напечатанных на 3D-принтере).Благодаря конструкционной металлической оболочке и легкому пластиковому сердечнику детали могут быть изготовлены с удивительно высокими характеристиками прочности на изгиб.
Помимо улучшения механических свойств, гальваническое покрытие можно использовать для защиты пластиковых деталей от воздействия окружающей среды. В тех случаях, когда пластиковые детали подвергаются химическому воздействию или ультрафиолетовому излучению, металлическое покрытие обеспечивает постоянный барьер, который может продлить срок службы ваших деталей с месяцев до лет.
При использовании в качестве эстетической обработки покрытие предлагает простой способ создания прототипов, которые одновременно выглядят и ощущаются как металл.В зависимости от толщины пластины гальванический пластик может быть тонким и легким или придавать изделию заметный вес. Более толстые гальванические покрытия можно даже текстурировать или полировать, чтобы получить различные металлические покрытия, от литого алюминия до зеркального хрома. Более сложные текстуры можно получить с помощью 3D-печати текстурированной подложки из смолы.
Учитывая потенциальные комбинации материалов для 3D-печати, различных металлов для покрытия и соотношений толщины листа, легко увидеть, как гальваническое покрытие дает инженерам новую область возможностей для проектирования.
Веб-семинарНа этом веб-семинаре вы узнаете, как гальваническое покрытие расширяет палитру материалов SLA 3D-печати для получения высокопрочных и износостойких деталей конечного назначения.
Посмотреть вебинар сейчасГальванопокрытие предлагает множество преимуществ, включая повышенную прочность, срок службы и проводимость деталей. Инженеры, производители и художники извлекают выгоду из этих преимуществ различными способами.
Инженеры часто используют гальваническое покрытие для повышения прочности и долговечности различных конструкций.Вы можете увеличить прочность на растяжение различных деталей, покрыв их металлами, такими как медь и никель. Поместите металлическую оболочку на детали, и вы сможете повысить их устойчивость к факторам окружающей среды, таким как химическое воздействие и УФ-излучение, для наружного или коррозионного применения.
Художники часто используют гальваническое покрытие, чтобы сохранить природные элементы, склонные к гниению, такие как листья, и превратить их в более прочные произведения искусства. В медицинском сообществе гальваническое покрытие используется для изготовления медицинских имплантатов, устойчивых к коррозии и поддающихся надлежащей стерилизации.
Гальваническое покрытие — это эффективный способ добавления косметической металлической отделки к изделиям, скульптурам, статуэткам и произведениям искусства. Многие производители также предпочитают гальваническое покрытие подложки для создания более легких деталей, которые легче и дешевле транспортировать и транспортировать.
Гальваническое покрытие также обладает преимуществом проводимости. Поскольку металлы по своей природе являются проводящими, гальваническое покрытие — отличный способ увеличить проводимость детали. Антенны, электрические компоненты и другие детали могут быть покрыты гальваническим покрытием для повышения производительности.
Хотя гальваническое покрытие имеет множество преимуществ, его ограничения заключаются в сложности и опасной природе самого процесса. Рабочие, занимающиеся гальванопокрытием, могут пострадать от воздействия шестивалентного хрома, если не примут надлежащих мер предосторожности. Рабочим необходимо иметь хорошо проветриваемое рабочее место. Управление по охране труда и гигиене труда Министерства труда США опубликовало множество документов, в которых описываются риски, связанные с гальванопокрытием.
Несмотря на то, что гальваническое покрытие полимерных деталей возможно выполнить самостоятельно, пользователи-любители могут столкнуться с трудностями.Основная причина — качество и возможности. Адгезионная прочность ламината с использованием методов гальванического покрытия своими руками обычно ниже, чем у профессиональных услуг по гальванике. Нанесение структурного покрытия, которое требует длительного времени обработки, нескольких ванн и совместимости металлов, довольно сложно выполнить надежно. Успешные применения внутреннего покрытия, как правило, просты и малы, например, прототипирование ювелирных изделий и тонкие (однослойные) медные покрытия RF.
Из-за требуемого опыта и связанных с этим опасностей многие инженеры и дизайнеры предпочитают нанимать стороннего производителя гальванических покрытий, специализирующегося на этом процессе.К счастью, несколько компаний, таких как RePliForm и Sharretts Plating, специализируются на индивидуальных проектах гальванического покрытия. Загрузите нашу белую книгу со списком гальванических услуг по регионам и объемам работ.
В приведенном выше видеоролике показано, как выполнять гальваническое покрытие с помощью легкодоступных инструментов, таких как зарядное устройство для мобильного телефона и запасная медная труба. Мы рекомендуем вам носить маску, перчатки и защитные очки во время гальванического покрытия и работать только в хорошо проветриваемом помещении.
Многие отрасли промышленности используют гальваническое покрытие для изготовления всего, от обручальных колец до электрических антенн.Вот несколько типичных примеров:
На многие детали самолетов нанесено гальваническое покрытие для добавления «защитного покрытия», которое увеличивает срок службы деталей за счет замедления коррозии. Поскольку компоненты самолета подвержены экстремальным перепадам температуры и факторам окружающей среды, к металлической основе добавляется дополнительный слой металла, чтобы функциональность детали не страдала от естественного износа.
Многие стальные болты и крепежные детали, разработанные для аэрокосмической промышленности, имеют гальваническое покрытие из хрома (или, в последнее время, из цинко-никелевого сплава в связи с изменением ограничений).
Введите слово «с гальванопокрытием» на Etsy, и вы получите огромное количество гальванического декора для дома и единственные в своем роде сувениры. С помощью этого процесса ремесленники часто превращают биоразлагаемые предметы, в том числе цветы, ветки и даже жуков, в прочные и долговечные произведения искусства. Вы можете использовать гальваническое покрытие, чтобы показать и сохранить мелкие детали в предметах, которые в противном случае быстро разложились бы.
Гальваника часто используется для создания произведений искусства, таких как медный жук и соты.(источник изображения)
Цифровые дизайнеры иногда используют гальваническое покрытие для создания скульптур. Дизайнеры могут 3D-печатать подложку с помощью настольного 3D-принтера, а затем гальванизировать дизайн медью, серебром, золотом или любым металлом по выбору для достижения желаемого результата. Комбинируя таким образом 3D-печать с гальванопокрытием, можно получить изделия, которые проще (и дешевле) в производстве, но при этом имеющие тот же внешний вид и отделку, что и скульптура из цельного литого металла.
Гальваническое покрытие очень распространено в автомобильной промышленности.Многие крупные автомобильные компании используют гальваническое покрытие для создания хромированных бамперов и других металлических деталей.
Гальваническое покрытие также можно использовать для создания нестандартных деталей для концептуальных автомобилей. Например, VW объединился с Autodesk для создания колпаков для своего концептуального автомобиля Type 20. Колпаки прототипа были напечатаны на 3D-принтере, а затем покрыты гальваническим покрытием.
Компании по реставрации и тюнингу автомобилей также используют гальваническое покрытие для нанесения никеля, хрома и других покрытий на различные детали автомобилей и мотоциклов.
Гальваническое покрытие, пожалуй, чаще всего ассоциируется с ювелирной промышленностью и драгоценными металлами. Дизайнеры и производители ювелирных изделий полагаются на этот процесс для улучшения цвета, долговечности и эстетической привлекательности колец, браслетов, подвесок и широкого спектра других изделий.
Когда вы видите ювелирные изделия, которые описываются как «позолоченные» или «посеребренные», велика вероятность того, что изделие, на которое вы смотрите, было гальванопокрытием. Комбинации различных металлов используются для получения уникальных оттенков отделки.Например, золото часто сочетают с медью и серебром для создания розового золота.
Гальваническое покрытие используется для придания упругости наружным поверхностям всех видов медицинских и стоматологических элементов. Золотое покрытие часто используется для создания зубных вкладок и помощи в различных стоматологических процедурах. Имплантированные детали, такие как сменные соединения, винты и пластины, часто покрываются гальваническим покрытием, чтобы сделать детали более устойчивыми к коррозии и совместимыми со стерилизацией перед установкой. Медицинские и хирургические инструменты, в том числе щипцы и радиологические детали, также обычно покрываются гальваническим покрытием.
На многочисленные электрические и солнечные компоненты нанесено гальваническое покрытие для повышения проводимости. Контакты солнечных элементов и различные типы антенн обычно изготавливаются с использованием гальванического покрытия. Провода могут быть покрыты серебром, никелем и многими другими металлами. Золотое покрытие часто используется (в сочетании с другими металлами) для увеличения долговечности. Золото также часто используется для увеличения срока службы деталей, потому что оно является проводящим, очень пластичным и не взаимодействует с кислородом.
Изготовление нестандартных или мелкосерийных металлических деталей для прототипирования может быть очень дорогостоящим и трудоемким при использовании традиционных производственных процессов.В результате инженеры часто комбинируют гальваническое покрытие с 3D-печатью, чтобы получить недорогое и экономящее время решение.
Например, Андреас Остервальдер из Швейцарского федерального технологического института в Лозанне (EPFL) смог ускорить процесс создания прототипов и снизить затраты на расширенные экспериментальные установки за счет самостоятельной 3D-печати новых конструкций на своем 3D-принтере Formlabs SLA и сотрудничества с Galvotec. гальванизировать эти детали.
Андреас Остервальдер использовал 3D-печать и гальваническое покрытие для изготовления этого светоделителя.
Антенны должны иметь электропроводность для распространения радиоволн. Пластиковые детали, напечатанные на 3D-принтере, не проводят электричество, но предлагают почти безграничную свободу дизайна и материалы с хорошими механическими и термическими свойствами. Эти преимущества можно сочетать с гальванопокрытием для достижения желаемой проводимости, в результате чего получается отличное решение для нестандартных антенн для исследований и разработок в автомобильной, оборонной, медицинской и образовательной областях.
При гальванике пластиковых деталей создаются проводящие детали, которые обеспечивают высокоэффективные радиочастотные приложения.
Композиты с гальваническим покрытием являются средством для достижения самых разных целей. Благодаря своей универсальности гальваническое покрытие открывает бесчисленные возможности в различных отраслях. Хотите узнать больше о гальванике 3D-печатных деталей?
Загрузите нашу белую книгу, чтобы узнать, как инженеры добавляют металл к 3D-печати из смолы и почему гибридные металлические детали могут открывать двери для удивительного диапазона применений, включая (но не ограничиваясь) конечной прочностью и долговечностью. К концу технического описания вы узнаете о новых способах нанесения гальванического покрытия, а также о проектных особенностях и практических советах по использованию металлического гальванического покрытия для повышения производительности ваших деталей SLA.
Демонстрация легкого гальванопокрытия меди для вашего окислительно-восстановительного агрегата
Мои старшие коллеги из IB заканчивают наш модуль по электрохимии и окислительно-восстановительному потенциалу. Это всегда было сложной темой в учебной программе IB. По общему признанию, электрохимия тоже никогда не была моей сильной стороной, поэтому в этом году я решил усилить модуль двумя дополнительными демонстрациями.
Летом я заказал аппарат Гофмана для демонстрации электролиза водных растворов. Когда я попробовал эту демонстрацию прошлой осенью, я обнаружил, что моя стеклянная посуда разбита.Но об этом я напишу в следующем блоге. Вместо этого я сосредоточусь на одной из самых простых демонстраций, которые я когда-либо создавал. Вот полный список оборудования и материалов:
- Стакан на 400 мл
- 200 мл 1 М CuSO4
- медный электрод
- Батарея 9 В
- Набор зажимов типа «крокодил»
- 1 скрепка
Рис. 1: Установка системы гальванического покрытия
Батарея 9 В обеспечивает необходимую энергию для запуска несамопроизвольного процесса в этой электролитической ячейке (см. рис. 1).Для демонстрации я подключил батарею и дал ячейке поработать около 30 секунд. Визуально мало что происходит. Но много всего происходит! Ионы меди в растворе восстанавливаются, покрывая скрепку красивым покрытием из относительно чистой меди. И медный электрод окисляется, таким образом заменяя ионы меди, которые покрывают скрепку. Это поддерживает концентрацию ионов меди в растворе на постоянном уровне.
Полуреакция окисления на медном аноде:
Cu
(s) —> Cu 2+ (водн.) + 2 e —
Полуреакция восстановления на катоде со скрепкой:
Cu
2+ (водн.) + 2 e- —> Cu (s)
На рис. 2 изображена скрепка с медным покрытием и чистым блеском части медного электрода, погруженной в раствор.Я провел электролиз всего около 30 секунд, но я хотел бы попробовать его на более длительное время и посмотреть, сколько меди покроет скрепку. У меня есть несколько миллиграммовых весов в моей комнате, чтобы проверить, можно ли также рассчитать скорость покрытия. В сценарии, где у меня было немного больше времени (и меньше необходимости так быстро продираться через учебную программу HL Chemistry), я хотел бы немного расширить это, чтобы студенты исследовали факторы, влияющие на скорость гальванического покрытия, такие как концентрация, напряжение и температура раствора.
Рисунок 2: Цинковая скрепка и медный электрод после 30 секунд гальванического покрытия
У вас есть расширения для этой демонстрации? Или предложения по дополнительным способам показать ученикам электролиз? Я хотел бы услышать об использовании вами этой или других демонстраций, связанных с электрохимией.
Меднение – обзор
Защита от коррозии
Как правило, большинство отказов технологического теплообменного оборудования является результатом локальной коррозии.Большинство отказов углеродистой стали происходит из-за отложений (подотложения/щелевая коррозия), омеднения (гальваническая коррозия) или биологического обрастания (MIC). Коррозия медных сплавов является результатом локальных отложений (подотложения/щелевая коррозия), высоких остаточных концентраций галогенов, используемых для микробиологического контроля, или сочетания галогенов и условий высокой солености. Щелевая и точечная коррозия являются наиболее распространенными механизмами разрушения нержавеющей стали [4].
Скорость и серьезность проникновения коррозии зависят от рабочей среды и материала, выбранного для применения.Например, углеродистая сталь может быть выбрана для оборудования с пониманием того, что общая коррозия будет прогрессировать постепенно и ее необходимо контролировать с помощью коррозионных купонов и датчиков коррозии. Конструктор может выбрать типичную нержавеющую сталь для теплообменника, не понимая, что условия низкого расхода могут вызвать отложения, которые могут привести к точечной коррозии под отложениями. Следовательно, скорость точечной коррозии трудно оценить, поскольку скорость загрязнения неизвестна, и ее особенно трудно контролировать с помощью коррозионных купонов.Это связано с тем, что купоны не должны подвергаться воздействию повышенных температур, низких скоростей потока и загрязнениям, фактически происходящим в пучке теплообменника. Большая часть оборудования для теплопередачи изготавливается из низкоуглеродистой стали из-за ее низкой стоимости и медного сплава из-за его высокой эффективности теплопередачи.
Системы водяного охлаждения обычно изготавливаются из более чем одного металлического сплава, каждый из которых обладает различными антикоррозионными свойствами. Когда железо подвергается коррозии, оно образует оксид железа, который препятствует потоку и выделяет растворимое железо (Fe 2+ ) в охлаждающую воду.Затем растворимое железо окисляется и образует нерастворимые соединения, которые загрязняют поверхности теплопередачи и снижают производительность процесса. Если коррозию меди не контролировать должным образом, растворимая медь, попадающая в охлаждающую воду, осаждается на стальных поверхностях. Образуются медно-железные (Cu/Fe) гальванические элементы, вызывающие точечную коррозию и приводящие к отказу оборудования. Для этих конструкционных материалов контроль и мониторинг коррозии требуют комплексного подхода к управлению, который может включать корректировку химического состава охлаждающей воды и/или рабочего pH, добавление биологических дезинфицирующих средств и выбор соответствующих ингибиторов коррозии.
Ингибитор коррозии – это любое вещество, которое эффективно снижает скорость коррозии при добавлении в окружающую среду. Анодные, катодные и смешанные ингибиторы представляют собой три типа ингибиторов коррозии.
Анодные ингибиторы (известные как пассиваторы) блокируют реакцию анодной коррозии, образуя защитный слой оксида (оксида железа) на поверхности металла. Это делает металлическую поверхность пассивной к коррозии. Наиболее распространенными пассиваторами стали являются нитрит, молибден и ортофосфат.Эти материалы являются неэффективными ингибиторами коррозии для меди и медных сплавов.
Катодные ингибиторы замедляют коррозию благодаря механизму осаждения, запускаемому локализованным высоким значением рН на катоде; осажденная пленка действует как микроскопический барьер, препятствующий переносу электронов с поверхности металла на растворенный кислород. Катодные ингибиторы или ингибиторы осаждения образуют соединения, которые нерастворимы при таком высоком значении рН (на 2–3 единицы рН выше, чем у основной массы воды), но осаждение которых можно предотвратить при значении рН основной массы воды (обычно 6.5–9). Соответствующий ингибитор осаждения/отложения необходим для обеспечения растворимости в объемной воде и предотвращения образования накипи на поверхностях теплопередачи. Ингибиторы осаждения не подходят для закрытых систем с длительным временем удерживания, поскольку даже хорошие ингибиторы осаждения не могут оставаться растворимыми. Примерами этих типов ингибиторов являются цинк, ортофосфат, полифосфат, фосфорорганические соединения (фосфонаты) и карбонат кальция. Цинк является наиболее эффективным ингибитором, поскольку он может осаждаться в виде гидроксида, фосфата и/или силикатной соли.
Смешанные ингибиторы абсорбируются на поверхности металла и образуют хемосорбированные пленки, которые одновременно блокируют очаги анодной и катодной коррозии.
Скорость коррозии увеличивается с увеличением проводимости воды (Рисунок 22-21). Хотя все ионные частицы вносят вклад в проводимость, анионы хлорида (Cl-) и сульфата (SO42-) являются наиболее вредными. Оба они ответственны за ускоренную коррозию в обработанной и неочищенной воде. На рис. 22-22 показана взаимосвязь между pH и скоростью коррозии железа.В очень кислом диапазоне pH (pH < 4) пленка оксида железа постоянно растворяется, и коррозия ускоряется реакцией восстановления водорода, которая является доминирующей катодной реакцией.
РИСУНОК 22-21. Скорость коррозии в зависимости от проводимости.
РИСУНОК 22-22. Скорость коррозии железа относительно постоянна.
Коррозию можно уменьшить, изменив металлургию или окружающую среду. Выбор сплавов, естественно устойчивых к общей коррозии, т.е. нержавеющей стали, может быть непомерно дорогим.Высоколегированные материалы также более склонны к разрушению из-за локальных механизмов коррозии. Изменение окружающей среды путем корректировки химического состава воды или добавления ингибиторов коррозии часто является наиболее широко применяемым методом борьбы с коррозией.
(22-10)2H++2e-→h3
При увеличении pH от 4 до 10 концентрация ионов водорода уменьшается, а карбонатная щелочность увеличивается. Это увеличивает возможность образования пленки карбоната кальция на катодных участках с высоким pH и подавления реакции коррозии.В отсутствие карбоната кальция скорость коррозии в диапазоне pH 4–10 относительно постоянна для любого заданного химического состава воды. Выше pH 10 железо становится все более пассивным. Кислород может быть основной движущей силой коррозии стали в охлаждающей воде. Увеличение коррозии с повышением температуры при заданной концентрации кислорода связано с более быстрой диффузией кислорода. Склонность воды к коррозии можно уменьшить путем механического или химического удаления кислорода. Хотя вакуумная деаэрация является подходящим средством для снижения уровня кислорода, химические поглотители чаще используются для закрытых систем, в которые практически не поступает воздух.Обычно используемые поглотители кислорода включают катализируемый сульфит натрия (Na 2 SO 3 ), гидроксиламин и аскорбиновую кислоту.





 Выбирается в зависимости от размера изделия.
Выбирается в зависимости от размера изделия.
 Обезжиривать сталь можно раствором из едкого натрия и едкого калия при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
Обезжиривать сталь можно раствором из едкого натрия и едкого калия при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой. На аноды замыкают положительную клемму.
На аноды замыкают положительную клемму.




 Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 °C. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 °C. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой. В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия. Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой. На аноды замыкают положительную клемму.
На аноды замыкают положительную клемму.
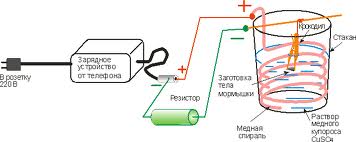


 Далее покрыть медью металл в домашних условиях будет не так трудно.
Далее покрыть медью металл в домашних условиях будет не так трудно.


 Реостатом добиваются необходимой силы тока из примерного расчета 10−15 миллиампер на каждый квадратный сантиметр площади детали.
Реостатом добиваются необходимой силы тока из примерного расчета 10−15 миллиампер на каждый квадратный сантиметр площади детали.
 Создаётся пластиковая или восковая основа, которую покрывают электропроводящим лаком и слоем меди. Подобную технологию меднения часто используют при изготовлении ювелирных изделий, сувениров, барельефов, матриц и волноводов.
Создаётся пластиковая или восковая основа, которую покрывают электропроводящим лаком и слоем меди. Подобную технологию меднения часто используют при изготовлении ювелирных изделий, сувениров, барельефов, матриц и волноводов.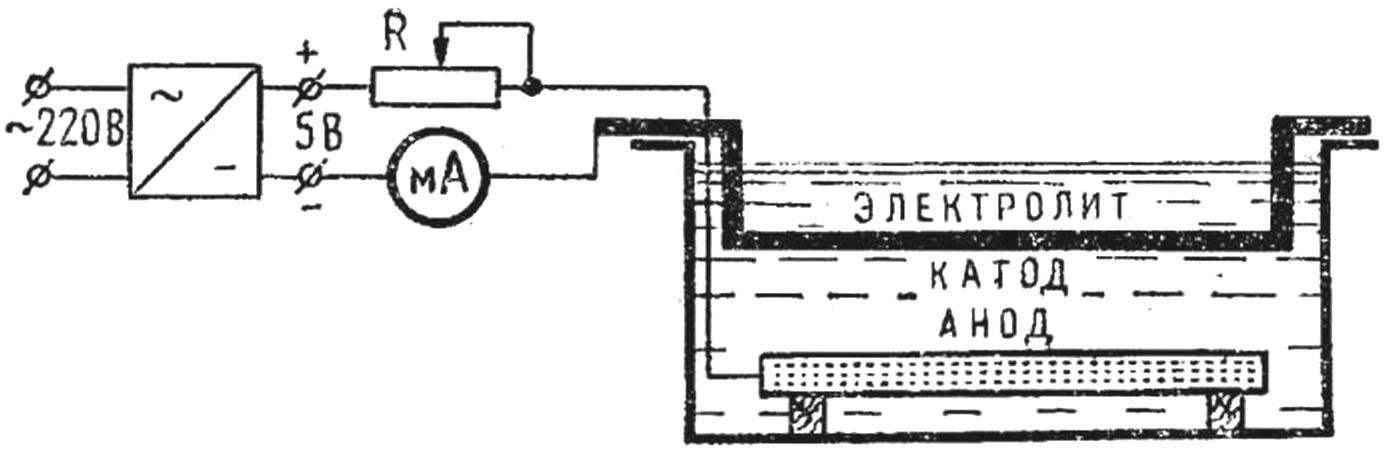
 Это действие позволяет обезжирить поверхность.
Это действие позволяет обезжирить поверхность.


